前面介紹了阿茲海默症的成因,以及粒線體、內質網等胞器和自噬作用異常時,都會促使病情惡化,並探討可能的機制與原因,而本篇將著重於患者治療的方法。雖然目前沒有完全治癒阿茲海默症的療法或藥物,但這些已經取得台灣 FDA 核准上市的藥物,仍然能維持或是改善患者的認知功能、減少行為混亂,並延緩疾病惡化。除此之外,本篇也將介紹標靶類澱粉蛋白質(amyloid)的免疫療法、tau 蛋白中心療法等。
FDA 核准上市藥物
Tacrine 為美國和台灣 FDA 於核准第一個使用在改善阿茲海默症認知功能並且明顯延緩疾病惡化的藥物,但因肝毒性副作用太強而下架,目前台灣 FDA 核准上市藥物,一類是膽鹼酶抑制劑(cholinesterase inhibitors),包括 donepezil、rivastigmine和 galantamine(表一),分別於 1997 年、2000 年、2001 年取得台灣 FDA 核准,用於治療輕度至中度阿茲海默症,而 2006 年 donepezil 取得核准用於治療重度阿茲海默症,由於這三種藥物抑制乙醯膽酯酶的水解作用,增加乙醯膽鹼之濃度,因而加強膽素性神經之功能,也可減緩澱粉酶原的前類澱粉蛋白質(Amyloid Precursor Protein,簡稱 APP)的形成,產生臨床治療效果,而且皆不需經由肝臟代謝,故不會造成肝毒性。另一類是 NMDA 受體(N-methyl-D-aspartate)拮抗劑 memantine(表一),memantine 可以防止 glutamate 的不正常傳導,進而改善認知功能。 FDA核准用於中至重度阿茲海默症,是目前唯一治療中度至中重度阿茲海默氏症的 NMDA 拮抗劑。
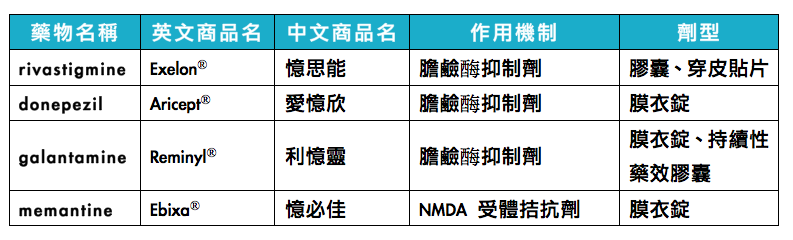
表一、台灣 FDA 核准治療阿茲海默症的藥物。(本表格由基因線上整理)
標靶類澱粉蛋白質的免疫療法
免疫療法主要是利用抗體來中和 β-類澱粉蛋白質(amyloid beta,簡稱 Aβ),治療阿茲海默症,而依抗體產生的方式不同,可分成主動性免疫接種和被動性免疫接種二種。主動性免疫接種為藉由疫苗刺激免疫系統而生成抗體。被動性免疫接種則是注射預製(pre-prepared)抗體。
主動性免疫接種參與細胞型和免疫體液型(humoral)免疫系統,具有成本效益和確保長期高抗體力價(antibody titers,代表抗體的含量)。最早主動免疫治療阿茲海默症的疫苗為 AN-1792,利用全長的 Aβ 1-42 多肽作為免疫抗原直接進行免疫治療,在小鼠實驗中表現出了良好的治療效果,但是在第二期臨床試驗中,引發嚴重的腦膜炎等副作用而被迫中止。目前許多第二代 Aβ 主動免疫疫苗正在進行第一期臨床試驗,包含諾華藥廠(Novartis)研發 CAD106(Aβ1-6 多肽)、楊森藥廠(Janssen)和輝瑞藥廠(Pfizer)共同研發的 ACC001 (Aβ1-6 多肽)、AC 免疫研發的 ACI-24 (Aβ1-15 多肽)、默克藥廠(Merck)研發的 V-950(Aβ1-15 多肽)、AFFiRiS 研發的 AD-02 (Aβ1-6 多肽)等。聯腦科學 (United Neuroscience)所研發的 UB 311 (Aβ1–14多肽)已經進入第二期臨床試驗。
然而,主動性免疫接種會導致多株抗體反應,專一性較被動性免疫接種差,因此被動性免疫接種預防 Aβ 堆疊、清除 Aβ 的效果也較佳。目前進入第一期和第二期臨床試驗的抗體請見表二,而目前已經進行第三期臨床試驗的被動性免疫接種抗體,包含 Biogen 研發的 Aducanumab、AC 免疫研發的Crenezumab、羅氏(Roche)藥廠研發的 Gantenerumab、禮來公司 (Eli Lilly)研發的 Solanezumab 等(表二)。
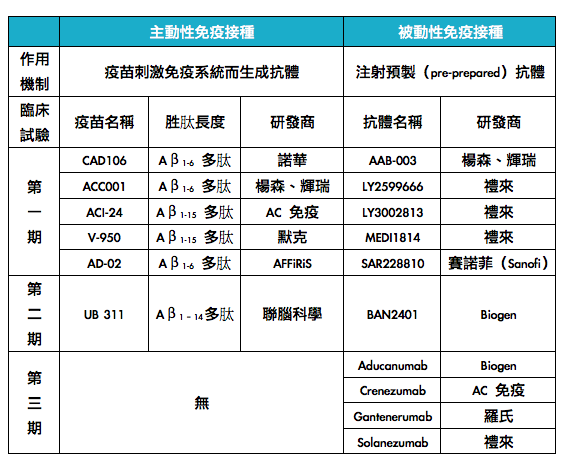
表二、主動性免疫接種和被動性免疫接種。(本表格由基因線上整理)
Tau 蛋白中心療法
Tau 蛋白過度磷酸化促使阿茲海默症的發生及惡化,因此以 tau 蛋白為中心的療法,包括 tau 蛋白激酶抑製劑、tau 蛋白堆疊抑制劑、微管穩定劑(microtubule stabilizers)和 tau 蛋白免疫療法,都有可能治療阿茲海默症(表三)。肝醣合成酶激酶-3(glycogen synthase kinase-3β,簡稱 GSK-3β)為 tau 蛋白磷酸化的最主要酵素,因此研究人員使用GSK-3β 抑制劑,如 tideglusib 和 AZD1080,進行臨床試驗,但結果顯示,AZD1080 具有腎毒性(nephrotoxicity)會造成腎臟受損,而 tideglusib 於第二期臨床試驗結顯示,沒有安全性問題,但也無法證實有療效。簡言之,目前仍未有療效佳且安全的 GSK-3β 抑制劑。
亞甲藍(methylthioninium chloride)衍生物 LMTC 可抑制 tau 蛋白之間的交互作用,進而促使 tau 蛋白從腦部清除。微管穩定劑 BMS241027(epothilone-D)也可抑制 tau 蛋白堆積,雖然有進行第一期臨床試驗,但也已經終止。
目前 tau 蛋白免疫療法,以預防神經纖維糾結(neurofibrillary tangles)形成為主要研究方向。Axon 神經科學公司所研發的 tau合成活性蛋白疫苗 AADvac1 和 AC 免疫與楊森共同研發的磷酸化 tau 蛋白特異性疫苗 ACI-35,皆能避免 tau 蛋白堆疊,目前分別進行入第二期和第一期臨床試驗。
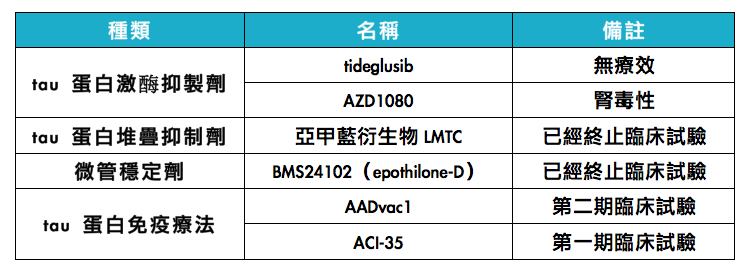
表三、Tau 蛋白中心療法。( 本表格由基因線上整理)
參考資料:
1. Jan AT, et al. Front Aging Neurosci. 2017 Nov 1;9:356. doi: 10.3389.
2. http://dlweb01.tzuchi.com.tw/dl/med/joural/journal59.pdf
3. https://www.fda.gov.tw/mlms/hlist.aspx
4. https://wwwfs.vghks.gov.tw/001/VghksUploadFiles/288/ckfile/cf50b729-93c5-4dd4-9db9-97dd1ca68c07.pdf
5. https://www.alzforum.org/therapeutics
6. http://adisinsight.springer.com/drugs/800027767
7. https://www.sciencedirect.com/topics/medicine-and-dentistry/methylthioninium-chloride
8. Wang CY, et al. Alzheimers Dement (NY). 2017 Apr 14;3(2):262-272
9. Wischik CM J Alzheimers Dis. 2015;44(2):705-20.
©www.geneonline.news. All rights reserved. 基因線上版權所有 未經授權不得轉載。合作請聯繫:service@geneonlineasia.com





