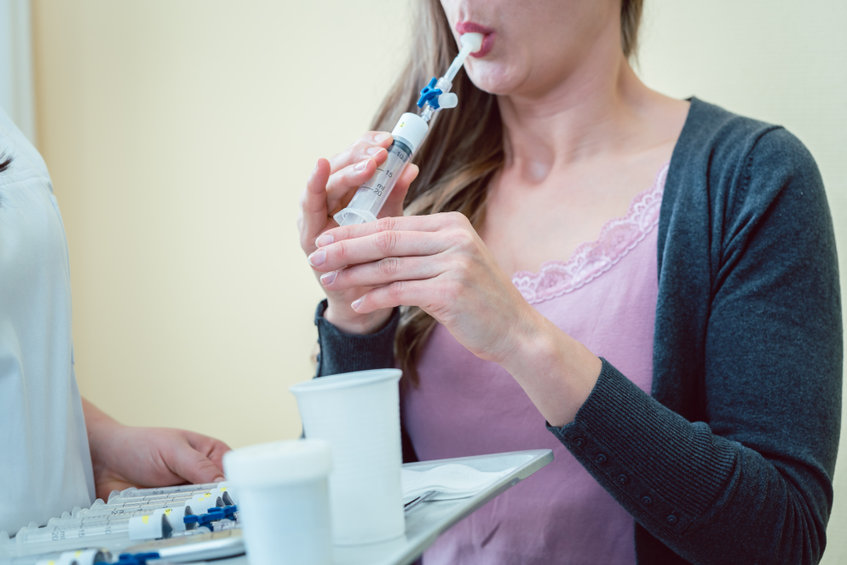
美國 FDA 於日前核准全球第一個新冠肺炎呼氣式分析儀(Breathalyzer) InspectIR COVID-19 的緊急使用授權(EUA),透過偵測受試者呼氣檢體內的化學物質來分析是否感染新冠病毒(SARS-CoV-2)。分析儀的尺寸約等同於一個手提式行李,方便經訓練的醫療人員在醫院、診間或快篩站進行檢測,並最快可在三分鐘內得知檢測結果。
InspectIR 預計每週生產約 100 台 COVID-19 呼氣式分析儀,每台儀器每日能分析約 160 個檢體,每月可檢測約 64,000 位受試者。
第四劑新冠 mRNA 疫苗的好與壞(基因線上國際版)呼氣分析儀檢測效率高,敏感性高達 91.2%
InspectIR 的 COVID-19 呼氣式分析儀早在 2020年新冠疫情甫爆發時就已宣布將進行臨床試驗,經歷兩年的努力,已順利在兩千多人的大型臨床試驗中證實具有 91.2% 的敏感性與 99.3% 的特異性,且陰性預測值(Negative Predictive Value, NPV,為檢測出陰性也的確沒患病的機率)高達 99.6%。
COVID-19 呼氣分析儀內建所使用的技術為氣相層析質譜儀(GC-MS),可分離與辨別混合的化學物質,以快速檢測出呼氣檢體中與新冠病毒感染有關的五種揮發性有機化合物(Volatile Organic Compounds, VOCs)。然而,FDA 指出呼氣分析儀的檢驗結果還是須以核酸檢測(PCR test)做最後確認,不應作為檢測的唯一依據。
FDA 樂見另類新冠快篩法研發
除了最常用的鼻腔採檢快篩法,FDA 也核准了其他另類的檢測法,以幫助快速篩檢新冠肺炎的感染狀況,包含 2020 年 5 月核准的唾液檢體快篩 SalivaDirect,與 2021 年 5 月緊急授權的手指採檢快篩 ADEXUSDx 等。
FDA 設備與放射健康中心主任 Jeff Shuren 醫師在聲明中表示道:「今日授權的新型 COVID-19 快篩法又是一個創新的好點子,因應疫情持續延燒,FDA 將會繼續支持新型 COVID-19 檢測的開發。」
延伸閱讀:借鏡 COVID-19 快篩開發經驗!牛津大學攜手香港 Prenetics 打造傳染病新世代快篩參考資料:
1. https://www.fda.gov/news-events/press-announcements/coronavirus-covid-19-update-fda-authorizes-first-covid-19-diagnostic-test-using-breath-samples
2. https://inspect-ir.com/inspectir-systems-begins-covid-19-detection-trial/
©www.geneonline.news. All rights reserved. 基因線上版權所有 未經授權不得轉載。合作請聯繫:service@geneonlineasia.com