双特异性抗体(Bispecific Antibodies, bsAb)为一种经由蛋白质工程技术将二种针对不同抗原的抗原结合片段(fragment of antigen binding, Fab)或单链变异区片段(single-chain variable fragment, scFv)结合成为一个抗体上的新型抗体药品,使其可同时与二种以上不同的抗原决定位(epitope)结合并具有专一性。双特异性抗体有多种形式,从相对较小的蛋白质(仅由两个连接的抗原结合片段组成)到具有附加结构域的大型类免疫球蛋白G(immunoglobulin G, IgG)分子。
三大优势胜过于单特异性抗体
与单特异性抗体相比,双特异性抗体的优势有三点。其一,它能将效应细胞直接标靶病变细胞,增强其细胞毒性。其二,它能同时分辨二种分子,提高抗体的选择性和功能性亲和力,然后改善药物的安全性和有效性。其三,过去需二种单特异性抗体药物联合用药治疗,现在透过双特异性抗体药物能减少开发和临床试验成本。
市场及临床现况
全球第一个上市的双特异性抗体 Removab(Catumaxomab)在 2009 年于欧洲获准上市,主要治疗已经出现恶性腹水(malignant ascites)症状的实体肿瘤,接着由于商业策略失败,销售额惨淡,2017 年退出市场进行重整,2018 年已在德国的 CMO 公司启动生产恢复,将于今年(2019 年)启动重新上市的申请以及新的适应症的开发。第二个上市的双特异性抗体 Blincyto(Blinatumomab)在 2014 年于美国获准上市,主要治疗急性淋巴性白血病。第三个上市的双特异性抗体 Hemlibra(Emicizumab)则在 2017 年在美国获准上市。其 2018 年的总销售额不到10亿美元。未来,将随着厂商不断开发出新的 BsAb 适应症,并且不断获得发展中和发展国家的药证上市。预计,到2025年 BsAb 的市场总值估计将超过 80 亿美元。
表一、目前核准上市的双特异性抗体
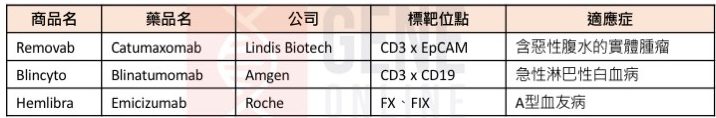
截至 2019 年七月,目前约有 224 种双特异性抗体正进行临床试验,以癌症治疗领域为最大宗,约占总额 86%(表二),其标靶位点又可细分为恶性血液肿瘤的 CD3、BCMA、CD123、 CD19、CD20、CD33、CD38,以及实体肿瘤的 DLL4、VEGF、HER2、PSMA、CAM。此外,由于近年来 CTLA-4、PD-1和PD-L1等免疫检查点抗体的成功,许多厂商也将正在开发含有这些免疫检查点的双特异性抗体。
表二、目前正在进行癌症治疗临床试验的双特异性抗体(只列出部分资讯)
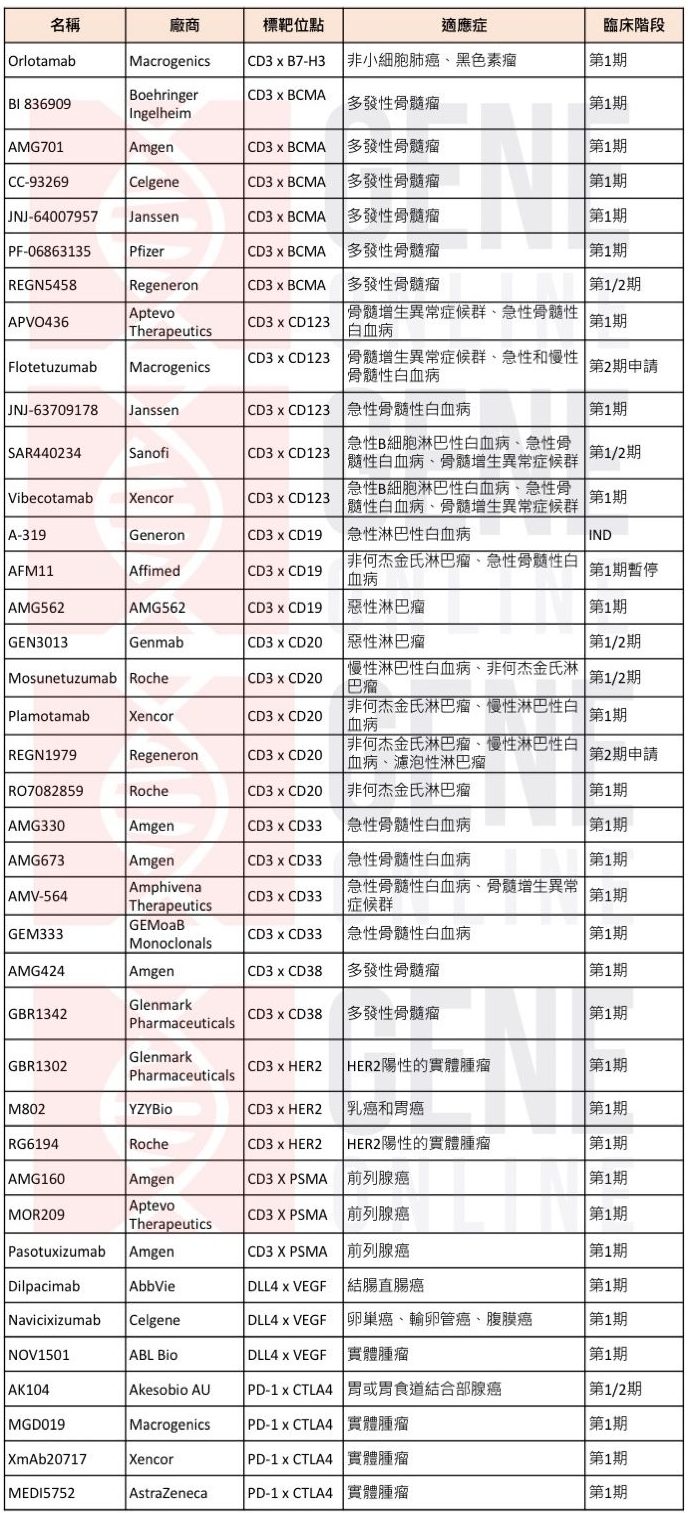
除肿瘤以外,治疗传染病、中枢神经系统病变、自体免疫性疾病等双特异性抗体也正在开发及进行临床试验中(表三)。
表三、目前正在进行非癌症治疗临床试验的双特异性抗体
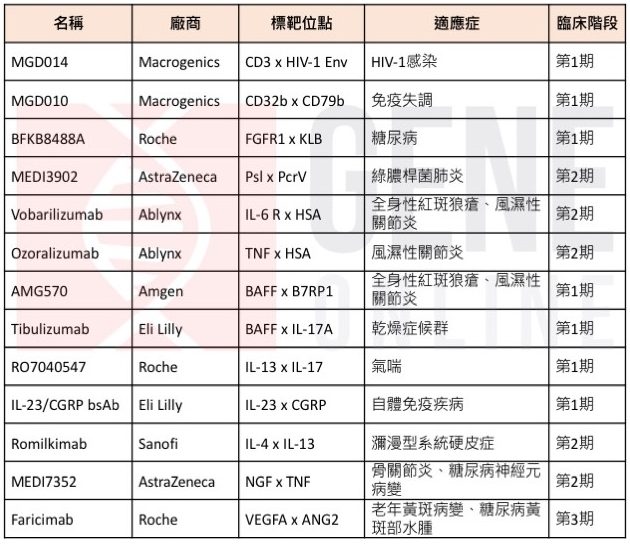
未来展望
总结以上,尽管与单特异性抗体相比,双异性抗体的复杂性在开发和临床等阶段都可能带来额外的挑战,但其有较佳的抗体的选择性和功能性亲和力,并且有较高的药物的安全性和有效性。虽然目前市场仅有三种双特异性抗体核准上市,但仍有二百多种正在进行临床试验,其中又以癌症治疗为最多,其次为免疫相关疾病。面对如此庞大商机,Roche、Amgen、Pfizer、Sanofi、Eli Lilly 等各大药厂以及 Ablynx、Macrogenics 等其他生技公司当然不会错过,纷纷投入研究开发。因此,紧追在免疫检查点抑制剂、CAR-T疗法之后,双异性抗体也是未来将在市场上显露光芒的药物之一。
延伸阅读:免疫疗法一时瑜亮! 双特异性抗体力拼 CAR-T参考资料:
1. Nature Reviews Drug Discoveryvolume 18, pages585–608 (2019)
2. https://www.researchandmarkets.com/research/xhhw54/global_bispecific?w=5
3. https://www.medgadget.com/2019/07/global-bispecific-antibody-market-offers-usd-8-billion-opportunity-with-200-drugs-in-clinical-trials.html
4. https://www.drugbank.ca/drugs/DB06607
5. https://www.accessdata.fda.gov/drugsatfda_docs/nda/2017/761083Orig1s000TOC.cfm
©www.geneonline.news. All rights reserved. 基因线上版权所有 未经授权不得转载。合作请联系:service@geneonlineasia.com





