mRNA 疫苗在新冠防疫上创造了巨大的成功,现今这项潜力科技也被延伸应用至爱滋病毒预防。爱滋病(后天免疫力缺乏综合症,AIDS)是因 HIV 病毒感染造成,患者免疫系统受到渐进式破坏,至今仍没有有效治愈方式。
一项由美国国家过敏及传染病研究所(National Institute of Allergy and Infectious Diseases, NIAID)、莫德纳(Moderna)联合研究指出,接种多剂 HIV 病毒的 mRNA 疫苗可使爱滋感染风险降低 79%,在恒河猴模型证实有效且安全性无疑虑。
mRNA 疫苗可转译两种 HIV 相关蛋白
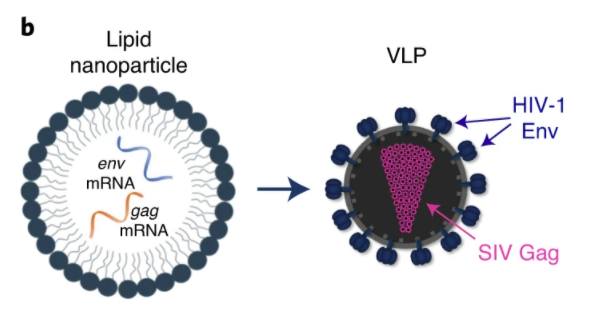
此 mRNA 疫苗的设计原理和新冠疫苗类似,只是将可转译出新冠病毒棘蛋白的 mRNA 片段,置换成 2 个与 HIV 生成有关的 Env、Gag 基因。Env 会转译出 HIV 外套膜,Gag 则会形成 HIV 病毒颗粒。
接种此疫苗后,Env、Gag 转译形成的蛋白会在动物体内产生类病毒颗粒(virus-like particles, VLPs),VLPs 只有 HIV 片段基因、不具有造成感染风险,但它们能够引发宿主动物的免疫反应。
小鼠、恒河猴模型分别证实有效
该研究分为小鼠、恒河猴模型两部份实验。首先,小鼠接种 2 剂 HIV 的 mRNA 疫苗,显示 VLP 平台技术产生的蛋白,能够模拟感染真实 HIV 病毒造成的免疫反应。
接着恒河猴模型中,恒河猴接种第 1 剂 HIV 的 mRNA 疫苗后,一年内又再施打追加剂量(500 μl)。为了更广泛标靶病毒蛋白,该疫苗带有的 Env、Gag 基因片段分别来自 HIV-1、以及猿猴免疫缺乏病毒(Simian immunodeficiency virus, SIV)。SIV 和 HIV-2 相似,且相较 HIV-1,非人类灵长动物更容易感染 HIV-2。
结果显示接种 58 周后,所有恒河猴产生的中和抗体,可标靶 12 种不同 HIV 病毒株。除此该疫苗也诱发辅助 T 细胞的免疫功能。
接种后第 60 周起,研究人员每周将恒河猴以直肠粘膜(rectal mucosa)暴露 SHIV 病毒。相较未接种疫苗恒河猴平均 3 周后就感染 HIV,实验组的平均感染时间延长至 8 周以后,执行至第 13 周时,7 只恒河猴中仍有 2 只未感染。
NIAID 病毒科科长 Paolo Lusso 表示,进一步证实该平台安全性后,未来该团队也计划展开人体 1 期临床试验。
莫德纳 mRNA 流感疫苗动态
另一方面,此研究的另一执行单位:mRNA 疫苗大厂莫德纳,近期也首度公告其流感疫苗 mRNA-1010 临床数据。该疫苗对 4 种流感病毒可成功产生中和抗体,不过和现有的减毒、蛋白质次单位流感疫苗相比,引发的副作用较严重。
莫德纳也表示将扩大研发 2 款四价流感疫苗。其中一项候选疫苗会比 mRNA-1010 多出一个血球凝集素(hemagglutinin, HA)抗原,另一则是 mRNA-1020 附加 2 个 HA 抗原。HA 糖蛋白为流感病毒附着宿主细胞的构造。
先前该公司也宣布正在开发次世代流感疫苗(mRNA-1020, mRNA-1030),将结合神经胺酸酶(neuraminidase)抗原以增强 HA 以外免疫作用。
延伸阅读:新兴科技“mRNA 疫苗”对付新冠病毒,能成为癌症治疗的新星?参考资料:
1. Nature Medicine, 2021; https://www.nature.com/articles/s41591-021-01574-5
2. https://www.niaid.nih.gov/news-events/experimental-mrna-hiv-vaccine-safe-shows-promise-animals
3. https://investors.modernatx.com/news/news-details/2021/Moderna-Announces-Positive-Interim-Phase-1-Data-for-mRNA-Flu-Vaccine-and-Provides-Program-Update/default.aspx
4. https://investors.modernatx.com/news/news-details/2021/Moderna-Provides-Business-Update-and-Announces-Three-New-Development-Programs-in-Infectious-Disease-Vaccines-01-11-2021/default.aspx
©www.geneonline.news. All rights reserved. 基因线上版权所有 未经授权不得转载。合作请联系:service@geneonlineasia.com