多重抗药性(multidrug resistance, MDR)是造成抗生素效果逐渐降低主因,与药物运输排出的量增加、排入的量减少有关。美国麻省理工学院(MIT)化学研究团队透过核磁共振(nuclear magnetic resonance, NMR)光谱,成功辨识出药物运输蛋白的结构是如何随着药物分子的移动而产生变化。未来将能藉抑制运输蛋白结构的转变以增加细菌的药物敏感性。此研究于日前刊登于 Nature Communications。
抗药性运输蛋白 SMR 家族
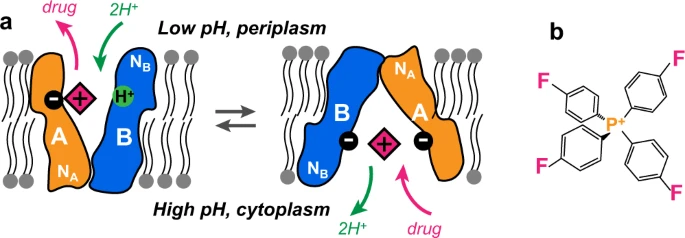
小分子多重抗药性(small multidrug resistance, SMR)运输蛋白家族透过在细菌细胞膜上高度表现,以增加药物排出增加而导致抗药性的产生。美国威斯康辛大学(University of Wisconsin)的 Henzler-Wildman 研究团队多年来一直致力于 SMR 运输蛋白家族中的 EmrE 的相关研究。EmrE 膜蛋白可以运输多种有毒分子,包含除草剂和抗菌化合物等。据研究发现,EmrE 将有毒分子从细菌细胞内(酸碱中性)运出细胞外(酸性),而 EmrE 的结构会根据酸碱值的改变而产生变化,进而确保有毒分子皆排出于细胞外。
来自 MIT 化学研究团队的 Mei Hong 教授的实验室近期开发出全新技术,透过核磁共振技术以测量蛋白质中氟与氢原子的距离,进而辨识有含氟分子结合的蛋白质结构。Henzler-Wildman 进而提出利用 Mei Hong 团队的核磁共振技术以探讨 EmrE 如何跨磷脂质膜运输药物分子。
运输蛋白随酸碱改变结构,增加药物排出效率
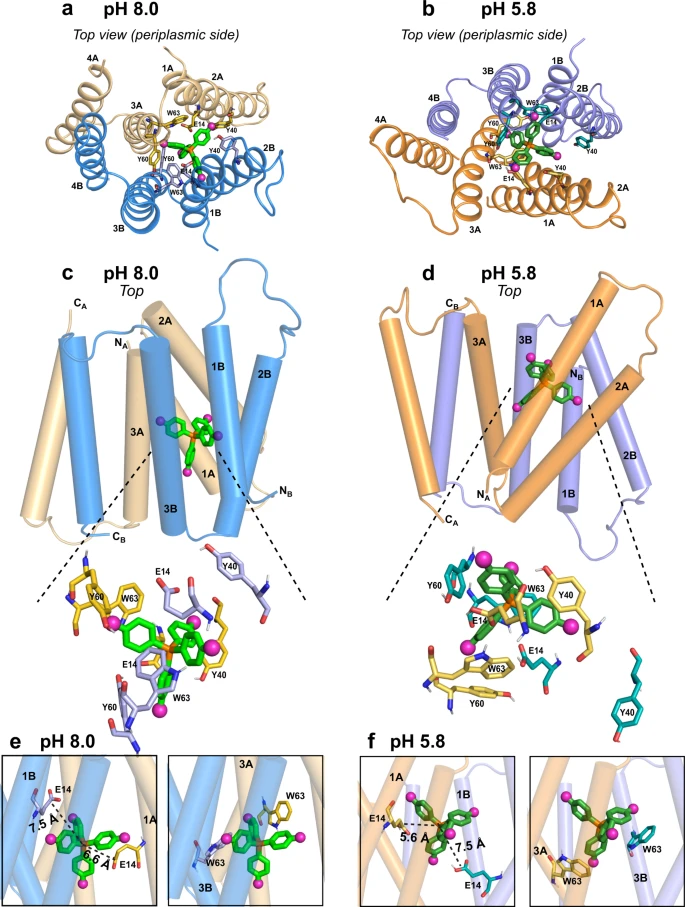
Hong 与 Henzler-Wildman的研究团队 于 2021 年合作发表的文献中指出,他们已成功透过核磁共振技术辨识出 EmrE 在酸性环境中的结构。而在本次发表的新研究中,成功分析出运输蛋白在中性酸碱值的结构,进而了解蛋白质的结构是如何在酸碱值变化中改变以排出药物分子。
在靠近细胞内、酸碱呈中性时,组成运输通道蛋白的四个螺旋体会排列成相对平行,进而形成一开口以方便药物从细胞内进入通道。而随着酸碱值逐渐降低(变酸)时,螺旋体会排列呈倾斜状,使通道向细胞外侧更开放;与此同时,蛋白质侧链的环状结构也会随着分子输出细胞外而不断改变,有利于药物分子的输出。
研究团队指出,透过分析蛋白质运输通道在酸性与中性的结构变化,可以更了解细菌是如何排除不利于自身的化学物质而产生抗药性。未来也会持续针对运输蛋白的结构变化做更多探讨,以设计出抑制结构转换的物质,进而改善抗药性。
延伸阅读:防堵细菌感染,用细菌载体攻破“生物膜”防护罩!参考资料:
1. https://www.nature.com/articles/s41467-022-28556-6
©www.geneonline.news. All rights reserved. 基因线上版权所有 未经授权不得转载。合作请联系:service@geneonlineasia.com