韩国基础科学研究所基因工程中心的研究人员,开发了一种新的基因编辑平台TALED(transcription activator-like effector-linked deaminases ),能够在粒线体中进行 A 到 G 碱基转换编辑。这项令人振奋的新发现,被认为是基因编辑技术中最后的临门一脚。
CRISPR-Cas 借由编辑基因组突变,开启治疗新道路
从 1968 年发现了第一个限制酶、1985 年发明了聚合酶连锁反应 (polymerase chain reaction, PCR) 、 2013 年 CRISPR 基因编辑,到近期的 TALEN(Transcription Activator-Like Effector Nuclease),生物技术的每一个新发现与突破,都进一步提高了人类改变世界的能力。
CRISPR 基因编辑可能有安全疑虑?(基因线上国际版)粒线体基因变异导致疾病
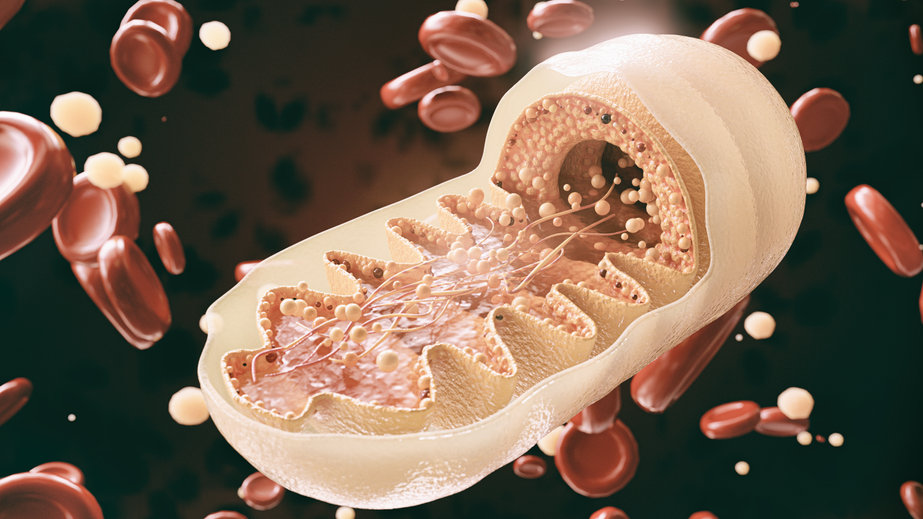
粒线体,即所谓的“细胞发电厂”,是细胞中的微小胞器,主要是由外膜、内膜与基质组成,负责供应细胞能量。由于它是能量代谢的重要细胞器,如果发生突变,就会引起与能量代谢相关的严重遗传疾病。
执行研究的基因组工程中心主任Kim Jin-Soo说:“由于粒线体的DNA缺陷,会出现一些极恶劣的遗传性疾病。例如,导致双眼突然失明的Leber氏遗传性视神经病变(Leber hereditary optic neuropathy, LHON),是由粒线体 DNA 的一个单点突变。”它会让患者的视线由一个小白点的遮蔽,逐渐扩散为大范围的白雾状,直到视线完全被遮蔽,目前医学上尚无法有效治疗这种神经退化性的遗传疾病。目前全世界的盛行率不明,而英国北部及芬兰的盛行率大约1/30,000~1/50,000。
另一种粒线体常见的基因疾病,乳酸血症和类中风症状的脑病变 (mitochondrial encephalomyopathy with lactic acidosis and stroke-like episodes, MELAS),是一种影响身体许多系统的疾病,特别是大脑、肌肉和神经系统。患者通常于2-10岁间陆续出现疾病相关的临床表征,可能包括肌肉无力和疼痛、反复头痛、食欲不振、呕吐和癫痫发作。大多数患有MELAS的人体内都有乳酸堆积,这种状况称为乳酸酸中毒,因血液酸度增加而导致呕吐、腹痛、极度疲倦、肌肉无力和呼吸困难等症状。
编辑粒线体 DNA 的技术演进
我们的基因一半来自父亲、一半来自母亲,唯独粒线体 DNA 一定来自母亲,因为在受精的过程当中,精子的粒线体基本上不会进入卵子。粒线体 DNA 中有 90 种已知的致病突变点,至少 5,000 人中的 1 人受此影响。
由于向粒线体传递基因方法受到限制,许多现有的基因组编辑工具无法使用。 例如,CRISPR-Cas 平台不适用编辑粒线体中的突变,因为引导 RNA 本身无法进入胞器。Kim Jin-Soo补充说道:“另一个问题是缺乏粒线体疾病的动物模型。因目前无法设计出建立动物模型所需的粒线体突变,使得开发和测试这些疾病的治疗方法变得非常困难。”
2020 年,由哈佛大学布罗德研究所( Broad Institute )和麻省理工学院的 David R. Liu 领导的研究人员设计了一种新的碱基编辑器,名为 “DddA ”衍生的胞嘧啶碱基编辑器 (derived cytosine base editors, DdCBEs),它可以从粒线体中的 DNA 进行 C 到 T 的转换。这是透过建立一种新的碱基编辑技术,将单个核苷酸碱基转换为另一个碱基而不破坏 DNA。然而,这种技术仅限于 C-to-T 转换,而且主要限于 TC,使其成为有效的 TC-TT 转换器。这意味着它只能修正 90 个中的 9 个( =10% )确认的致病性粒线体点突变。
TALED 能进行 DNA A-to-G 转换
这篇公布于Cell研究的第一作者 Cho Sung-Ik 说:“为了克服这些限制,我们能够建立了一个名为 TALED 的新型基因编辑平台,以实现 A-to-G 转换。新平台扩大了粒线体基因编辑的范围,不仅可以建立疾病模型,也可以为开发治疗做出重大贡献。”值得注意的是,仅能够在人类 mtDNA 中进行 A 到 G 转换就可以纠正 90 种已知致病突变中的 39 种(= 43%)。
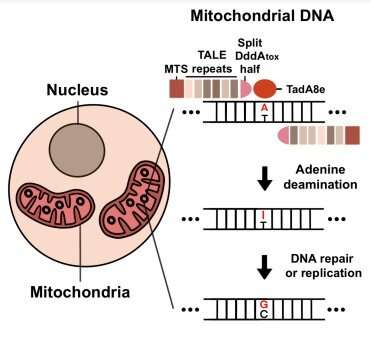
研究人员融合三个不同的成分创造了 TALED。 第一个成分是转录类活化因子效应遗传因子 (transcription activator-like effector, TALE),它能够瞄准 DNA 序列。第二个成分是 TadA8e,一种促进 A 到 G 转换的腺嘌呤去氨酶。第三个成分 DddAtox 是一种胞嘧啶去氨酶,它使 TadA8e 更容易接近 DNA。有趣的是研究团队发现 TadA8e 能够在具有双股 DNA 的粒线体中进行 A 到 G 编辑,和过去所知 TadA8e 是一种仅对单股 DNA 具有特异性的蛋白质不同。Kim Jin-Soo表示,以前没有人想过使用 TadA8e 对粒线体进行碱基编辑,因为认为它应该只针对单股 DNA。这种跳出框架的思维模式,帮助拓展了新的领域。
研究人员推测,DddAtox 允许通过极短的时间窗口打开双股,让 TadA8e,这种快速酶进行必要的编辑。除了调整 TALED 的成分外,研究人员还开发了一种能够同时进行 A-to-G 和 C-to-T 碱基编辑以及仅 A-to-G 碱基编辑的技术。他们透过建立包含所需粒线体 DNA(mtDNA)编辑的单细胞衍生复制,来展示这项新技术。此外,因 TALED 既没有细胞毒性,也不会导致 mtDNA 不稳定,脱靶效应也很少,研究人员希望透过提高编辑效率和特异性来进一步改进 TALED,为胚胎、胎儿、新生儿或成年患者引起疾病的 mtDNA 突变,开创新的道路。
延伸阅读:故障的“细胞发电机”?第一个活体内基因编辑治疗粒线体疾病参考资料:
- http://www.tfrd.org.tw/tfrd/library_b2/content/category_id/1/id/954
- https://phys.org/news/2022-04-era-mitochondrial-genome-begun.html
©www.geneonline.news. All rights reserved. 基因线上版权所有 未经授权不得转载。合作请联系:service@geneonlineasia.com