今年癌症聯合學術年會的主題聚焦於癌症的精準醫療(Precision Medicine),患者在接受治療之前,透過基因檢測或液態生物檢體(Liquid Biopsy)分子檢測就能預先評估選擇最適當的治療方法,有望大幅提升治療效率並節省無效醫療的資源浪費。
副總統當選人陳建仁於5月14日出席這場會議時指出,未來推動精準醫療需要大數據,並提倡「4P 醫學」,即預防醫學(Preventive)、預測醫學(Predictive)、個人化醫學(Personalized)及參與醫學(Participatory)。將家族病史、病毒感染、環境暴露等因子數據化,預測罹病風險及治療效果後,再給予個人化治療,不僅能降低不必要的健保支出,也可提升癌症存活率。
腫瘤治療大躍進 邁向精準醫療
臺大醫院 郭文宏醫師表示,乳癌的手術治療雖然顯著 (74~88%),但仍有術後復發的風險,以往僅能從病灶型態與病理組織來推測復發風險,現在則可以透過基因檢測 (Oncotype DX、Mammaprint、PAM50、Endopredict等) 預估手術後復發風險與是否需要接受化學治療或荷爾蒙治療,甚至預先挑選使用對患者效果較顯著且副作用較低的化療藥物,提升治療品質。
根據加拿大研究,在 2433 名乳癌患者的身上找到 40 個腫瘤抑制基因 (Tumor Suppressor gene) 和致癌基因 (Oncogene) 突變,這些基因都在細胞訊息傳遞路徑扮演重要驅動功能。然而,從乳癌患者的腫瘤組織做基因分析發現,平均帶有 1.57 個基因序列突變,這些突變都極有潛能成為新的標靶治療標的,成為臨床個人化醫療的新契機。未來甚至透過腫瘤細胞釋放到血液中的微量 ctDNA(circulating tumor DNA)偵測,就能夠及早檢查出腫瘤的生成或是治療後監控腫瘤復發。
延伸閱讀: 液態生物檢體國際權威齊聚一堂 2016 ELBA 會後報導液態生物檢體與癌症免疫治療(Cancer Immunotherapy)
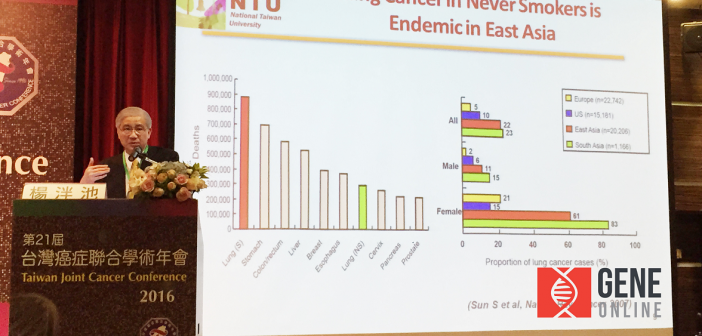
臨床肺癌研究權威,現任台灣大學校長楊泮池醫師提到,精準癌症科學 (Precission Oncology) 和精準醫療的新時代已經來臨,現代分子檢測的進展:次世代基因定序、Panomics、液態檢體的生物標記 (Biomarkers of liquid biopsy samples) 、生物大數據演算平台等技術都逐漸成熟,全球也早已開始建立跨國癌症基因體研究組織和計畫,例如: International Cancer Genome Consortium(IGCG) 、The Cancer Genome Atlas (TCGA),提升癌症治療的成效。
現代的癌症治療可分為:風險評估、早期診斷、精準治療三個階段,以肺癌為例,透過胸部X光或斷層掃描可偵測到 0.5~1.0 公分的腫瘤 (109 Cells),但若透過液態生物檢體的一些生物標記例如: ctDNA或 CTCs(Circulating Tumor Cells),則有助於腫瘤的更早期監測與輔助診斷,並提高患者接受手術後追蹤的意願和效率。
近年來的肺癌標靶治療趨勢,除了針對亞洲人好發的 EGFR 突變的 TKI 抑制劑外,還有癌症免疫治療的生物標記 (PD-1、PD-L1、CTLA-4) 藥物發展,也相當令人期待。來自美國的 Bernard A. Fox 博士舉例,光是 2015 年美國食品藥物管理局 (FDA) 就批准了兩種針對 PD-1 免疫治療在肺癌的臨床使用。今年二月,免疫療法 (Immunotherapy) 更被美國臨床腫瘤學會 (American Society of Clinical Oncology)定為 2016 年臨床癌症發展的重要里程碑。
大數據演算 掀起臨床醫療革命
隨著 DNA 基因定序效率平均每 7~18 個月(超越 Moore`s rule)成長一倍的進展速度,我們已經能夠運用大量基因體生物資訊演算找到 正確的標的、藥物、患者、時間。仰賴大數據演算的四大核心價值: 數量 (Volume)、多元性 (Variety)、速度 (Velocity)、準確性 (Veracity) ,讓精準醫療的核心價值得以實現。
德州大學安德森癌症中心所領導參與的「癌症登月計畫」(Cancer Moonshot Program) 範疇涵蓋:個人化癌症治療、早期偵測與診斷、臨床基因體學(Clinical Genomics)、免疫治療、基因體資訊學 (Genomics Informatics) 、大數據分析等方面,應用在 12 種癌症的治療,目標是透過精準治療策略減低癌症患者的死亡率和痛苦。
雖然癌症是基因疾病,但由於腫瘤細胞之間的基因異質性 (Heterogeneity) 高、訊息傳遞路徑和成因複雜,若要實現癌症的精準醫療必須整合基因體學 (Genomics)、蛋白質體學 (Proteomics)、代謝體學 (Metaboliomics) 和 X-Omics 等面向,才能全方位評估癌症,達成精準醫療的目標。
綜觀今年的學術研討主題,可彙整出下列趨勢:
1. 基因檢測等分子診斷技術將與臨床癌症預防、治療產生密不可分的唇齒關係,例如癌症用藥的伴隨式診斷(Companion Diagnostics)將蔚為風潮。
2. 非/低侵入性早期診斷方法例如液態生物檢體,將是臨床分子檢測的發展重點。
3. 免疫細胞調節與癌症免疫治療,將是癌症臨床新藥發展的重要方向。
4. 生物資訊演算與大數據分析,將可望輔助臨床醫療人員精準判斷,提升醫療效率。
5. 提倡精準醫療,大幅減少無謂的醫療資源浪費。
©www.geneonline.news. All rights reserved. 基因線上版權所有 未經授權不得轉載。合作請聯繫:service@geneonlineasia.com
延伸閱讀:美國總統向癌症宣戰! 全力推動抗癌登月計畫(Cancer Moonshot)參考文獻:
1. The somatic mutation profiles of 2,433 breast cancers refines their genomic and transcriptomic landscapes. Nature Communications 7, Article number: 11479.
2. Development and validation of a clinical cancer genomic profiling test based on massively parallel DNA sequencing. Nature Biotechnology 31, 1023–1031 (2013).
3. Immunotherapy: The 2016 Clinical Cancer Advance of the Year. 4. http://www.cancer.net/blog/2016-02/immunotherapy-2016-clinical-cancer-advance-year
4. 「癌症登月計畫」(Cancer Moonshot Program). http://www.cancermoonshots.org/