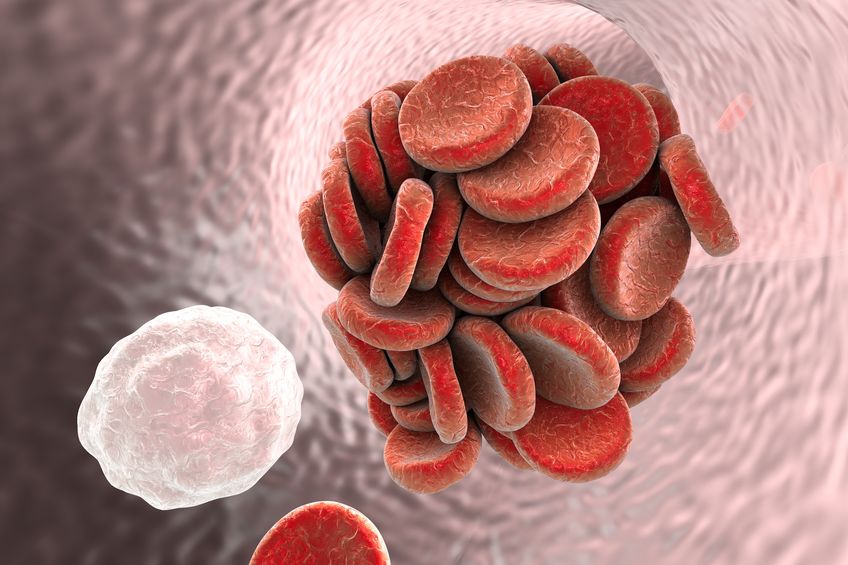
嚴重新冠肺炎(COVID-19)患者不僅可能會產生嚴重的呼吸道發炎問題、細胞激素風暴,還有一半以上的患者在其動脈、靜脈和微血管中出現血栓,限制肺中的血流來誘導中風,並損害氧氣交換,嚴重時更會猝死。
近日,密西根大學弗蘭克爾心血管中心的研究團隊發現,這些 COVID-19 患者的致病性自身抗體過度表現和嗜中性白血球過度活化,是其發生血栓的主要原因。相關研究結果刊登於《Science Translational Medicine》。
這些引起血栓的抗體能標靶「磷脂和磷脂結合蛋白」(phospholipids and phospholipid-binding proteins, aPL),所以被稱為 aPL 抗體,常見於抗磷脂症候群(antiphospholipid syndrome,一種自身免疫性疾病)的患者中。
aPL 抗體與嗜中性白血球過度活化與血栓形成有關
該研究團隊檢測172名因 COVID-19住院的患者血清中的 8 種 aPL 抗體,包括抗心磷脂 IgG、IgM 和 IgA、抗 β2 醣蛋白 I IgG、IgM 和 IgA,以及抗磷脂醯絲胺酸(Phosphatidylserine)/凝血酶原(aPS / PT)IgG 和 IgM。然後,他們在24% 的血清檢體中檢測到 aPS / PT IgG,在 23% 的檢體中檢測到抗心磷脂IgM,在 18% 的血清檢體中檢測到 aPS / PT IgM。使用製造商的閾值來分析,抗磷脂自身抗體存在於 52% 的血清檢體中,若使用更嚴格的臨界值(≥40個ELISA特異性單位)存在於30%的血清檢體中。
再來,他們更發現較高滴度的 aPL 抗體與嗜中性白血球過度活化有關,包括釋放嗜中性白血球胞外網狀結構(neutrophil extracellular traps, NETs),更高的血小板數量,更嚴重的呼吸系統疾病和較低的臨床估計腎小球濾過率。另外,與抗磷脂症候群患者的 IgG 相似,從 COVID-19 患者中分離的 IgG 組分促進了從健康個體中分離的嗜中性白血球胞外網狀結構釋放。
動物試驗發現,aPL 抗體誘導血栓形成
在 2 個小鼠模型中,將從 COVID-19 患者血清中純化的 IgG 注射到小鼠中可加速靜脈血栓形成。該研究通訊作者 Jason Knight 醫學博士表示:「本研究發現,有一半的 COVID-19 住院患者有此致病性抗體,這很令人驚訝。另外,我們將此抗體打入小鼠體內,引起了驚人的凝結,這是我們見過的最嚴重的凝結。因此,我們推測這些抗體就是引起血栓的主因。」
該研究作者 Yogen Kanthi 醫師表示:「自身致病性抗體與 COVID-19 之間的聯繫是出乎意料的。在 COVID-19 患者中,我們繼續看到一個無情且自我放大的發炎循環和體內凝血。本研究結果使我們了解,自身抗體可能是這種凝血和發炎循環的罪魁禍首,這讓原本就很掙扎的人染上了更重的疾病。」
抗凝血老藥 dipyridamole,有抗 COVID-19 發炎的潛力
該研究團隊也正進行一項名為DICER的隨機臨床試驗,主要在 COVID-19 患者中測試一種著名的抗凝血劑 dipyridamole,以確定其在減少過多血凝塊方面是否比安慰劑更有效。Kanthi 醫師表示,dipyridamole 是一種安全,廉價且可擴展的藥,FDA 早於 20 年前核准它來預防凝血,但他們直到最近才發現它阻止這種在COVID-19 發炎的潛力。
延伸閱讀:面對 COVID-19 重症凝血異常難題! 國際臨床專家如何應對?參考資料:
1. Science Translational Medicine 02 Nov 2020: eabd3876.DOI: 10.1126/scitranslmed.abd3876
2. https://labblog.uofmhealth.org/lab-report/new-cause-of-covid-19-blood-clots-identified
©www.geneonline.news. All rights reserved. 基因線上版權所有 未經授權不得轉載。合作請聯繫:service@geneonlineasia.com