雙特異性抗體(Bispecific Antibodies, bsAb)為一種經由蛋白質工程技術將二種針對不同抗原的抗原结合片段(fragment of antigen binding, Fab)或單鏈變異區片段(single-chain variable fragment, scFv)結合成為一個抗體上的新型抗體藥品,使其可同時與二種以上不同的抗原決定位(epitope)結合並具有專一性。雙特異性抗體有多種形式,從相對較小的蛋白質(僅由兩個連接的抗原結合片段組成)到具有附加結構域的大型類免疫球蛋白G(immunoglobulin G, IgG)分子。
三大優勢勝過於單特異性抗體
與單特異性抗體相比,雙特異性抗體的優勢有三點。其一,它能將效應細胞直接標靶病變細胞,增強其細胞毒性。其二,它能同時分辨二種分子,提高抗體的選擇性和功能性親和力,然後改善藥物的安全性和有效性。其三,過去需二種單特異性抗體藥物聯合用藥治療,現在透過雙特異性抗體藥物能減少開發和臨床試驗成本。
市場及臨床現況
全球第一個上市的雙特異性抗體 Removab(Catumaxomab)在 2009 年於歐洲獲准上市,主要治療已經出現惡性腹水(malignant ascites)症狀的實體腫瘤,接著由於商業策略失敗,銷售額慘淡,2017 年退出市場進行重整,2018 年已在德國的 CMO 公司啟動生產恢復,將於今年(2019 年)啟動重新上市的申請以及新的適應症的開發。第二個上市的雙特異性抗體 Blincyto(Blinatumomab)在 2014 年於美國獲准上市,主要治療急性淋巴性白血病。第三個上市的雙特異性抗體 Hemlibra(Emicizumab)則在 2017 年在美國獲准上市。其 2018 年的總銷售額不到10億美元。未來,將隨著廠商不斷開發出新的 BsAb 適應症,並且不斷獲得發展中和發展國家的藥證上市。預計,到2025年 BsAb 的市場總值估計將超過 80 億美元。
表一、目前核准上市的雙特異性抗體
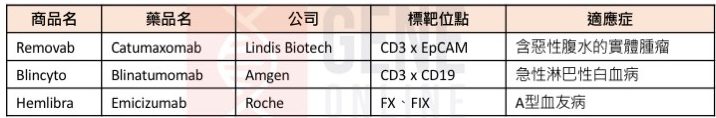
截至 2019 年七月,目前約有 224 種雙特異性抗體正進行臨床試驗,以癌症治療領域為最大宗,約佔總額 86%(表二),其標靶位點又可細分為惡性血液腫瘤的 CD3、BCMA、CD123、 CD19、CD20、CD33、CD38,以及實體腫瘤的 DLL4、VEGF、HER2、PSMA、CAM。此外,由於近年來 CTLA-4、PD-1和PD-L1等免疫檢查點抗體的成功,許多廠商也將正在開發含有這些免疫檢查點的雙特異性抗體。
表二、目前正在進行癌症治療臨床試驗的雙特異性抗體(只列出部分資訊)
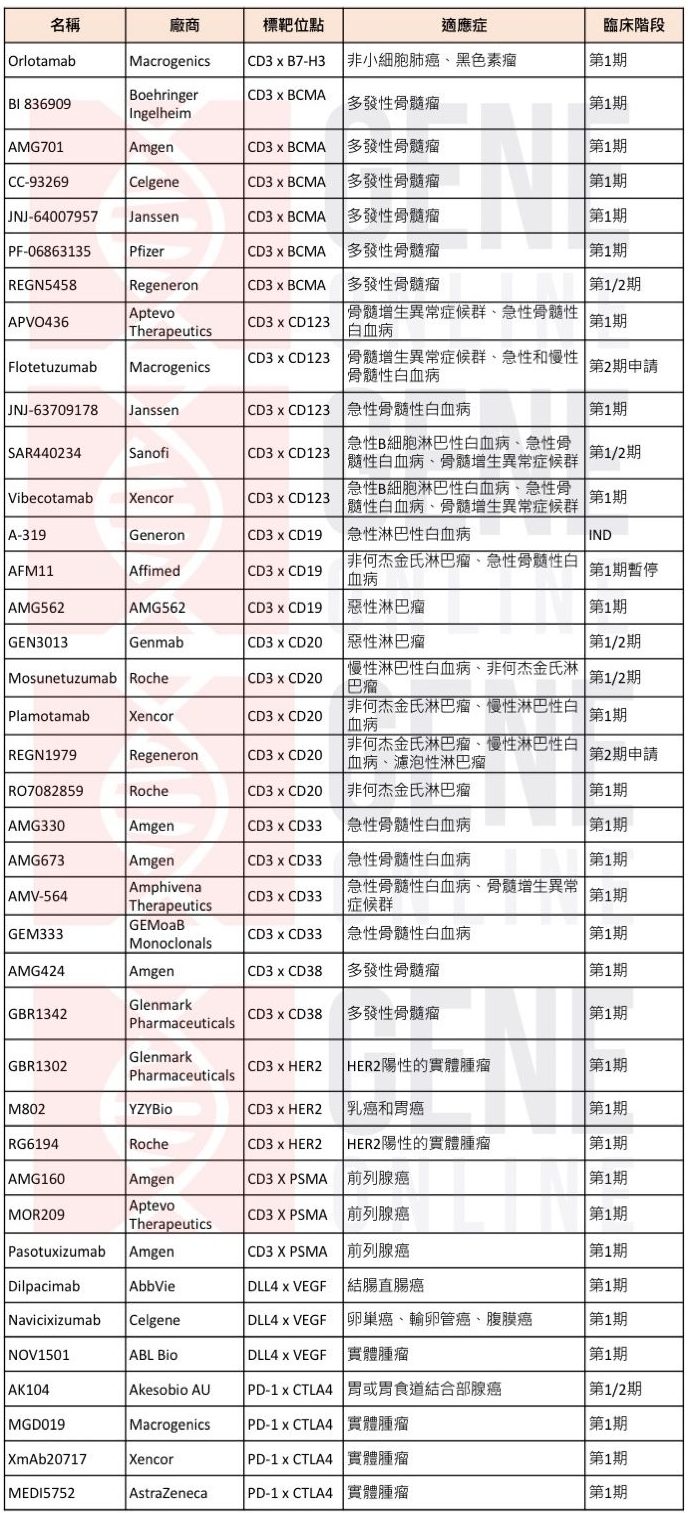
除腫瘤以外,治療傳染病、中樞神經系統病變、自體免疫性疾病等雙特異性抗體也正在開發及進行臨床試驗中(表三)。
表三、目前正在進行非癌症治療臨床試驗的雙特異性抗體
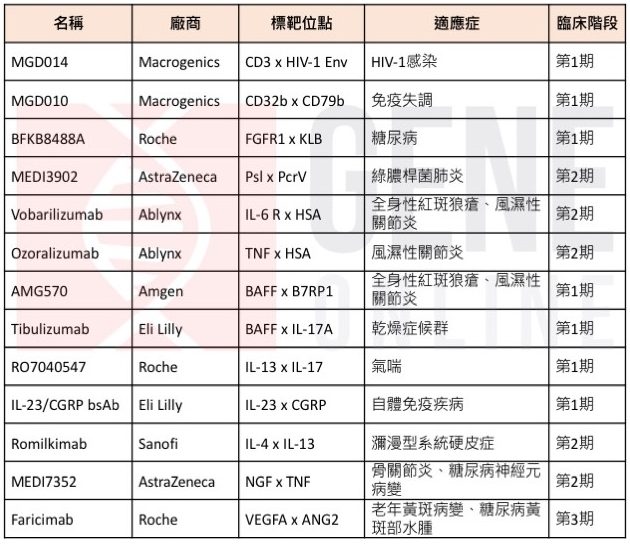
未來展望
總結以上,儘管與單特異性抗體相比,雙異性抗體的複雜性在開發和臨床等階段都可能帶來額外的挑戰,但其有較佳的抗體的選擇性和功能性親和力,並且有較高的藥物的安全性和有效性。雖然目前市場僅有三種雙特異性抗體核准上市,但仍有二百多種正在進行臨床試驗,其中又以癌症治療為最多,其次為免疫相關疾病。面對如此龐大商機,Roche、Amgen、Pfizer、Sanofi、Eli Lilly 等各大藥廠以及 Ablynx、Macrogenics 等其他生技公司當然不會錯過,紛紛投入研究開發。因此,緊追在免疫檢查點抑制劑、CAR-T療法之後,雙異性抗體也是未來將在市場上顯露光芒的藥物之一。
延伸閱讀:免疫療法一時瑜亮! 雙特異性抗體力拼 CAR-T參考資料:
1. Nature Reviews Drug Discoveryvolume 18, pages585–608 (2019)
2. https://www.researchandmarkets.com/research/xhhw54/global_bispecific?w=5
3. https://www.medgadget.com/2019/07/global-bispecific-antibody-market-offers-usd-8-billion-opportunity-with-200-drugs-in-clinical-trials.html
4. https://www.drugbank.ca/drugs/DB06607
5. https://www.accessdata.fda.gov/drugsatfda_docs/nda/2017/761083Orig1s000TOC.cfm
©www.geneonline.news. All rights reserved. 基因線上版權所有 未經授權不得轉載。合作請聯繫:service@geneonlineasia.com





