在組織和腫瘤環境中都可發現 T 細胞和其細胞表面 T 細胞受體(T cell receptor,簡稱 TCR) 的蹤影,它們能調控長效、抗原特異性、效應功能反應(effector response)和免疫記憶反應(memory response)。因此在免疫治療中,它們扮演相當重要的角色。
T 細胞受體的組成與功能
TCR 為調節 T 細胞的抗原特異性活化的多單元穿膜複合物(multi-subunit transmembrane complex),由 TCRα 和 TCRβ 鏈等二條不同的多肽鏈組成,可形成異質雙體,依其結構上所形成的不同功能區,可分為細胞膜外側的 N 端可變區(variable region)、恆定區(constant region)與重鏈區(H region),而利用穿膜區(transmembrane region)插於細胞膜上以及膜內側的短細胞質端。二鏈之間通過二硫鍵(disulphide bond)連接,每個受體提供單個抗原結合位點。
TCR 藉由辨識由抗原呈現細胞(antigen presenting cells,簡稱 APCs)上的主要組織相容性複合體(major histocompatibility complex,簡稱 MHC)所呈現的抗原配體,賦予 T 細胞抗原特異性。T 細胞表現的輔助性黏附分子 CD4 和 CD8 也參與在其中,其中 CD4 和第 II 型 MHC 形成的抗原複合體進行輔助辨識,而 CD8 和第 I 型 MHC 形成的抗原複合體進行輔助辨識。TCR 雙體在細胞內合成後,需要 CD3γ 、CD3δ、CD3ε、CD3ζ 等 4 種分子組成的複合體(包含 CD3δε 和 CD3γε 等二個異源二聚體以及同源二聚體 CD3ζζ)的協助,才能來到細胞表面。接著,CD3 複合體與 TCR 在 T 細胞表面形成一個穩定且具功能的 TCR 複合體,當 T 細胞遇到抗原時,此 T 細胞複合體中的 TCR 若辨識抗原成功,會透過 CD3 複合體將訊息傳遞到細胞內部,以啟動新蛋白質的合成,進而促使原始 T 細胞進行分裂與分化成作用 T 細胞、輔助性 T 細胞以及毒殺性 T 細胞,來擊退外來的病原,如細菌、病毒或癌細胞。
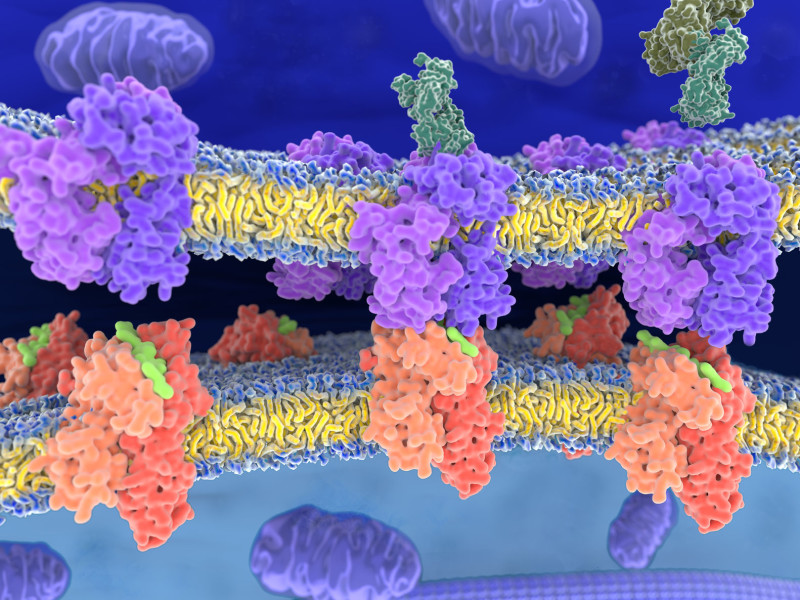
TCR 藉由辨識由抗原呈現細胞上的第二型 MHC 所呈現的抗原配體,賦予 T 細胞抗原特異性。
TCR 基因修飾於腫瘤治療之應用
T 細胞在胸腺內發育時,其 TCR 與自體內源自蛋白質之胜肽呈高親和力結合時,這些 T 細胞會被摧毀,此過程即稱為負面選擇(negative selection),就會產生中心耐受性。腫瘤環境也在免疫反應中起關鍵作用,腫瘤細胞可能會有躲避機制,使抗原呈現細胞不能完全接觸 TCR,而 T 細胞無法活化,產生周圍耐受性。因此,科學家透過修飾 TCR 基因提升 TCR 腫瘤抗原辨識能力,克服中心耐受性和周圍耐受性的限制,進而準確標靶具有特定抗原的腫瘤細胞,達到治療的效果,成為近幾年熱門研究方向。
修飾的 TCR 基因療法是透過表達特異性 TCRα 和 TCRβ 鏈來改變 T 細胞特異性。腫瘤特異性 TCRα和 TCRβ 鏈經辨識、分離以及複製到轉導載體中,並且轉導 T 細胞產生腫瘤抗原特異性 T 細胞。
為了成功產生腫瘤特異性TCR,需要確認合適的標靶序列,這可能從罕見的腫瘤反應性 T 細胞中分離出來,主要有三種方法。第一種方法是透過人類腫瘤蛋白表達人類白細胞抗原(human leukocyte antigen,簡稱 HLA)系統的轉殖基因小鼠,產生包含人類抗原辨識能力的 TCR 的 T 細胞。另一種方法是異體移植(allogeneic)TCR 基因轉移,其中腫瘤特異性 T 細胞從腫瘤緩解的患者中分離,並且反應性 TCR 序列從另一個無治療反應的患者的 T細胞轉移到 T 細胞。最後一種方法,體外技術(in vitro)可以用來改變 TCR 的序列,進而提升反應性腫瘤特異性 TCR 與標靶抗原的交互作用,增加 T 細胞擊殺腫瘤的活性。
延伸閱讀:免疫治療於癌症之應用T 細胞受體結合人工智慧 癌症治療大跨步
目前許多免疫療法都建立在已知的抗原基礎上,但對於這些抗原的屬性以及識別它們的 T 細胞,但仍有許多不清楚之處。為了解決這樣的疑問,約翰霍普金斯大學(Johns Hopkins University)醫學院研究團隊利用人工智慧(Artificial Intelligence,簡稱 AI)創建一套包含各種 TCR 性質的圖譜資料庫。
該研究團隊收集實驗室中暴露於病毒的人類 TCR 的基因組序列數據,並使用高性能計算技術來創建一個數字模型(本質上是一個數字地圖),他們的目標是聚集相似的 TCR,並可能標靶相同的抗原。他們接著透過無監督學習演算法(unsupervised learning algorithm),能夠根據受體序列中的相似性將 TCR 定序數據轉換為數字距離,並且依它們的功能特異性而聚集。例如,如果二個受體序列相似,則電腦則會在兩個序列之間分配短距離級別。如果序列不同,他們收到一個更長的距離排名。一旦數以千計的序列被轉換成這些“距離”度量,電腦系統的 AI 演算法能在受體之間尋找運作模式。
該研究團隊也透過在有腫瘤和無腫瘤的小鼠中,創建了腫瘤抗原特異性 TCR 多樣性的 ImmunoMap,其中接近腫瘤的 T 細胞樣本中 TCR 的多樣性比較遠。這些數據可能有助於未來研究團隊確定腫瘤如何逃避免疫系統的檢測。然而,該研究團隊 Jonathan Schneck 博士指出,該研究組還需要積累更多的 ImmunoMap 數據,才能準確地預測哪些患者對免疫療法才會有效。他也指出,對任何個體患者的免疫療法反應來說,ImmunoMap 不能將 TCR 與特定抗原配對成功或確定哪些抗原能配對成功,都是很重要的事。最後也希望 ImmunoMap 未來能有助於治療癌症的疫苗、T 細胞和 TCR 工程化的研發。
延伸閱讀:2017 CSCO系列報導(一):腫瘤大數據與人工智慧的應用文 / Parker Yang
參考資料:
1. Xing, Y. and Hogquist, K. A. T-cell tolerance: central and peripheral. Cold Spring 2. Harb. Perspect. Biol. (2012). 4, a006957.
3. Sharpe M and Mount N. Dis Model Mech. 2015 Apr;8(4):337-50.
4. Stanislawski T, et al. Nat. Immunol. 2001;2, 962–70.
5. Gao L, et al. Blood. 2000; 95, 2198–203.
6. Schmid DA, et al. J. Immunol. 2010;184, 4936–46.
7. Cancer Immunology Research, 2017; canimm.0114.2017 DOI: 10.1158/2326-6066.CIR-17-0114
8. http://dmm.biologists.org/content/8/4/337
9.https://www.health-holland.com/project/2017/t-cell-receptor-gene-therapy-of-cancer
10. http://idv.sinica.edu.tw/ibswcy/immunology/NTOU9.pdf
11. http://life.nthu.edu.tw/~bioclass/files/980111%20class-1.pdf
12. https://www.sciencedaily.com/releases/2018/01/180108101346.htm
©www.geneonline.news. All rights reserved. 基因線上版權所有 未經授權不得轉載。合作請聯繫:service@geneonlineasia.com





