自 2015 年时任总统欧巴马在国情咨文演说提出“精准医疗倡议 (Precision Medicine Initiatives,PMI)”以来,全球掀起精准医疗的热潮,尤其在癌症、肿瘤医学领域的应用进展迅速蓬勃。2016 年 9 月,美国国家研究所主导进行“癌症登月计划”与台湾、加拿大、中国、德国、瑞士、日本、韩国等七国合作,大规模蒐集检体进行癌症临床研究,更奠定了癌症治疗走向精准医疗的基础。今年五月初,第 22 届台湾癌症联合学术年会 (TJCC) 以“精准医疗的创新与进展 (Innovation & Advances in Precision Medicine)” 为主题,汇集产、学、研、医近千位专家齐聚国防医学院,在台湾大学校长杨泮池教授与台北医学大学校长阎云教授的引言中揭开序幕。
癌症精准医疗时代来临 基因检测扮演要角
癌症是一群源自基因的疾病,基因检测在临床的诊断 (Diagnosis) 、治疗 (Therapeutics)、预后 (Prognosis)和疾病监控 (Disease monitor) 等四大面向都扮演着关键角色。
针对今年大会,年会主席、也是中华民国妇癌医学会理事长的刘文雄表示,去年的主题也是精准医疗,但今年可望透过更多专业人士参与,互相激荡其创新理念与最新研究成果,找出更有效的个人化治疗方案,造福更多癌症病患。

Roche-Foundation Medicine 的医疗主管 James Creeden 博士
会议中来自 Roche-Foundation Medicine 的医疗主管 James Creeden 博士 (MD PhD) 表示,目前基因检测的应用已经成熟,肿瘤组织可透过基因定序建立完整基因体分析 (Comprehensive Genomic Profiling) ,再经由数据数据库的比对出可行的见解。例如:Foundation One 透过独特的 Hybrid Capture 技术将肿瘤基因体完整捕获可精准分析 315 个癌症基因的改变。包括: 1.单点突变 (Base Substitutions) 、2. 插入/重复序列(Insertion/Deletion)、3.拷贝数变化 (Copy number alteration)和 4.基因融合/重排 (Gene Fusion/Rearrangement) 等四大面向,相较于一般 PCR 基因热点检测,可增加目标基因变异的侦测率。但是,James Creeden 博士提醒,医师在参考基因检测分析结果给出临床治疗方针之前,尤其是药品仿单标示外使用 (Off-Label Use),最好要求检测单位提供验证数据 (Validated Data) 作为评估的依据,对于患者权益比较有保障。
液态生物检体 (Liquid Biopsy) 成肿瘤医学新显学
近年兴起的液态生物检体 (Liquid biopsies) 临床检测与研究,由于仅需经由体液采样(例如:血液、唾液或尿液)进行分析,具有低侵入性的优点,也为癌症甚至其他重大疾病的早期侦测诊断开启了新的契机。一般而言,Liquid Biopsies 可大致分为三个范畴:
- Circulating Cell Free DNA(cfDNA)/ Circulating Tumor DNA(ctDNA)
- Circulating Tumor Cells(CTCs)
- Circulating Exosomes 或 Extracellular Vesicles (EVs)
液态检体 (Liquid biopsies) 的发展以 Circulating Tumor Cells (CTCs) 检测最早,从 1990 年代就开始有侦测Circulating Tumor Cells (CTCs) 的纯化技术,但自从 2007 – 2008 年间次世代基因定序 (NGS) 问世以后,让cfDNA/ctDNA 的临床应用进展开始突飞猛进。
合度精密(CellMax Life) 首席科学官 Rui Mei 博士
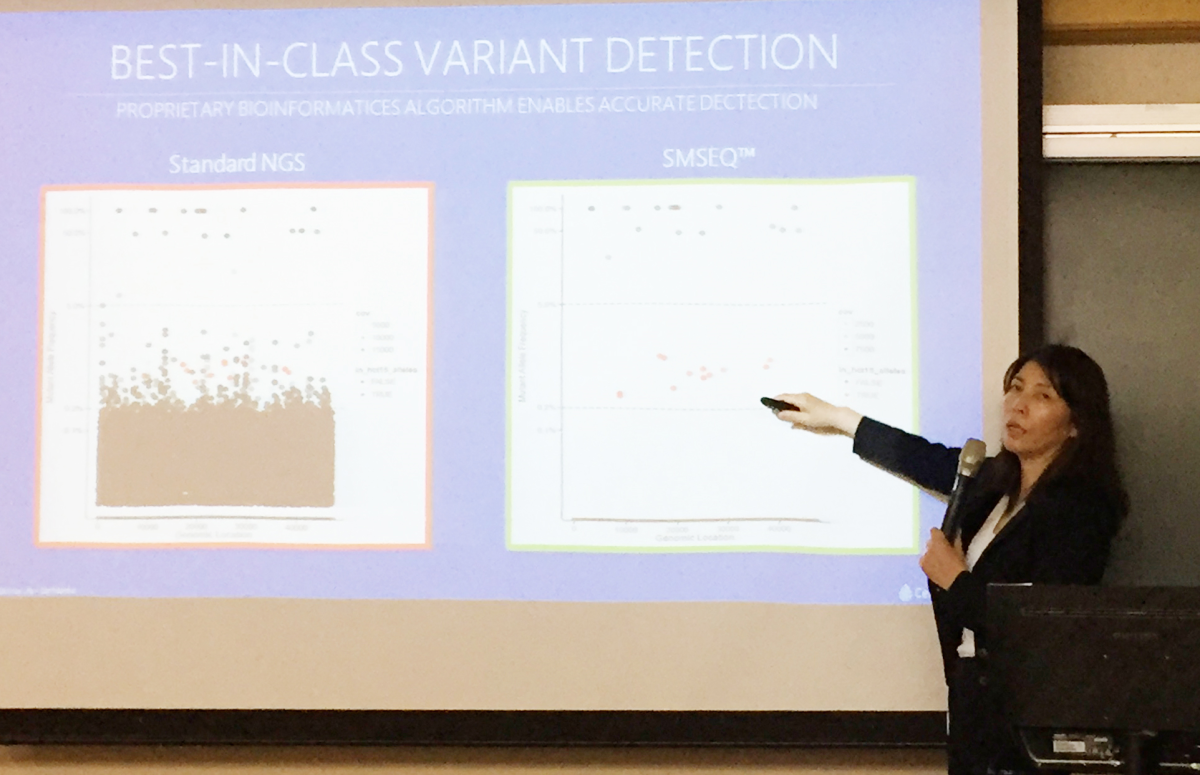
液态检体知名公司合度精密 (CellMax Life) 首席科学官 Rui Mei 博士于演讲中表示,CellMax 液态切片透过非侵入性、常态的抽血,可从循环肿瘤 DNA (ctDNA) 中分析出根据 NCCN Guideline 之 73 组基因,来判断评估临床上可治疗的基因变异。此检测使用 CellMax Life 专利的 SMSEQ 平台:此平台在捕捉、放大及分离 ctDNA 上均经过优化,且其特殊之 Silico Gene Panel 上可针对癌症相关侦测点做更深入的定序和探测,平均最高定序深度可达 20000X。相较于一般检测平台 ctDNA 的比例须达 0.5% 才能检测、且针对治疗性基因之侦测有高达 25% 的遗漏机率,OncoLBx 不仅在侦测 ctDNA 的极限比例可降至 0.1% (相对灵敏度较高),专一性也高达 99.999%,搭配临床比对 (annotation) 数据库,合度精密在台湾已有 500 多例癌症患者的临床数据统计,约有 78% 的受检者体内可以测得 ctDNA 变异,具不错的临床应用价值。Rui Mei 博士也强调,利用 SMSEQ 的平台,相较于其他平台,可大幅提升对基因片段缺失/重复 (Deletion/Insertion) 或基因融合/重排 (Gene Fusion/Rearrangement) 的灵敏度。

台湾癌症全人关怀基金会董事长 谢瑞坤 医师
台湾癌症全人关怀基金会董事长谢瑞坤医师则提到,因为 ctDNA 的半衰期短 (<2小时),血液内侦测到的 ctDNA 含量/基因突变能够代表体内肿瘤的即时状况,且根据研究在 14 种侵袭性高的肿瘤型态中有 80% 可侦测到 ctDNA 的存在。就临床经验而言,ctDNA 的参考价值甚至高过侵入性的肿瘤组织切片,因为组织切片的分析结果仅能代表当时的肿瘤状态,但 ctDNA 却能即时动态监测肿瘤行为 (Tumor Behavior),解决了肿瘤异质性 (Heterogeneity)造成传统肿瘤组织切片经常结果不一致造成误判的困扰。因此,谢医师相当推崇术后 / 治疗后采用 Liquid Biopsy 方法 (ex:ctDNA) 来监控肿瘤治疗效果与复发情形,给予精准的医疗决策。
台湾大学俞松良教授说明,目前 cfDNA/ctDNA 在临床主要的应用有二:(一)疾病的侦测辨识 (二)治疗后复发的监控/二线治疗 (second line treatment) 评估。最好的例子就是非小细胞肺癌患者使用标靶药物可能遇到“抗药性”,接受 EGFR T790M 突变的 ctDNA 检测若呈现阳性,就可考虑改用第三代 EGFR-TKI 药物治疗,目前已被美国国家癌症资讯网 (National Comprehensive Cancer Network ;NCCN) 列入临床指引。
行动基因 (ACT Genomics) 的陈淑贞博士则分享数年来的临床经验,在使用 NGS-based 定序深度 1000X 的前提下,涵盖 409 个与癌症相关的基因,近乎有八成的受检者能够检出可有药物治疗的基因变异,对于临床治疗提供了更多的可能性。ctDNA 的优点可用于术后肿瘤残量评估、监控肿瘤复发、评估药物治疗效果、追踪侦测肿瘤抗药性基因突变的发生,甚至未来可能应用于肿瘤的早期侦测。
精准肿瘤学 (Precision Oncology) 科技导向多元发展

美国 UCSF 的 John K.Chan 教授
来自美国 UCSF 的 John K.Chan 教授提出癌症治疗走向精准化与个人化主要拜因于两大因医素:(一)基因体导向的介入治疗 (二)精准治疗方法进展(标靶用药、放射治疗、外科手术)。标靶药物的开发最主要依循三大方向:基因体不稳定性与突变、免疫功能失效、血管新生。以最近热门的 BRCA 突变为例,BRCA1/BRCA2 基因突变而致的遗传性乳癌与卵巢癌,会特别倚赖 Poly (ADP-ribose) polymerase (PARP) 酵素来修补受损的基因,若使用 PARP 抑制剂来破坏此一酵素的作用,使癌细胞无法修补化疗造成的基因破坏,而使癌细胞更易受到药物的毒杀走向凋亡,目前美国食品药物管理局 (FDA) 已经核准数种 PARP 抑制剂新药上市,尤其对于被检测出 BRCA 突变的患者治疗效率尤佳。另外,针对免疫调节点 PD-1 和 PDL-1 的单株抗体也是近来相当受到瞩目的标靶治疗新药。总结来说,基因定序 / 检测的进展得以让临床治疗找到一些肿瘤生物标记 (Tumor Biomarkers) 、筛选对患者最有效率的药物、适切的治疗时机、有效 / 有害药物剂量,进而实现“个人化精准肿瘤学 (Personalized Precision Oncology)”。
另一方面,先进放射医疗技术也扮演关键的角色,例如:质子治疗 (Proton Therapy) 能精准定位肿瘤位置(精确度可达 0.01 毫米),集中能量对于肿瘤进行治疗而减少对于正常组织的影响。
高精密度的机器人手术 (Robotic Surgery) 搭配具肿瘤组织专一性的萤光染色显影技术,则能够让外科医师在进行手术时以最小的伤口精准地将带有萤光的肿瘤组织完整切除干净,降低术后复发风险,大幅提升手术治疗效率。
综观本届的台湾癌症联合学术年会,可归纳出未来癌症医疗领域的三大趋势:
- 科技导向的精准医疗。日益发达的精密工业、基因定序分析技术与人工智能,将可辅助提升医疗人员在医疗决策、手术、药物治疗、疾病防治等各方面的效率和精准度,大幅节约医疗资源浪费,提升大众医疗品质。
- 液态生物检体 (Liquid Biopsy)。主要可应用于肿瘤术后监测、药物/手术后疗效评估和癌症极早期侦测,侵入性低、取得容易的体液分析将逐步取代传统穿刺组织采样,成为精准医疗服务链当中非常重要的一环。
- 免疫标的导向的新药开发与治疗。肿瘤细胞必须逃脱免疫机制的监控才能顺利形成肿瘤,因此透过以免疫节点 (例如:PD-1、PDL-1、CTLA4) 或肿瘤细胞表面抗原(糖基)为调控机转的标靶治疗药物甚至免疫细胞辅助治疗将会持续有新的进展。

有鉴于液态生物检体 (Liquid Biopsy) 的基础研究与临床应用发展日益蓬勃,今年“第二届 Exosomes and Liquid Biopsies 亚洲国际研讨会”将于六月份在台湾举办,届时将汇集数百位来自欧洲、美国及亚洲的学者及专业人士齐聚一堂,共同研讨液态生物检体 (Liquid Biopsy) 令人振奋的最新进展,敬邀各位读者一同前来共赴这场知识的盛宴!
©www.geneonline.news. All rights reserved. 基因线上版权所有 未经授权不得转载。合作请联系:service@geneonlineasia.com






