前面介绍了阿兹海默症的成因,以及粒线体、内质网等胞器和自噬作用异常时,都会促使病情恶化,并探讨可能的机制与原因,而本篇将着重于患者治疗的方法。虽然目前没有完全治愈阿兹海默症的疗法或药物,但这些已经取得台湾 FDA 核准上市的药物,仍然能维持或是改善患者的认知功能、减少行为混亂,并延缓疾病惡化。除此之外,本篇也将介绍标靶类淀粉蛋白质(amyloid)的免疫疗法、tau 蛋白中心疗法等。
FDA 核准上市药物
Tacrine 为美国和台湾 FDA 于核准第一个使用在改善阿兹海默症认知功能并且明显延缓疾病惡化的药物,但因肝毒性副作用太强而下架,目前台湾 FDA 核准上市药物,一類是胆碱酶抑制剂(cholinesterase inhibitors),包括 donepezil、rivastigmine和 galantamine(表一),分别于 1997 年、2000 年、2001 年取得台湾 FDA 核准,用于治疗轻度至中度阿兹海默症,而 2006 年 donepezil 取得核准用于治疗重度阿兹海默症,由于这三种药物抑制乙酰胆酯酶的水解作用,增加乙酰胆碱之浓度,因而加强胆素性神经之功能,也可减缓淀粉酶原的前类淀粉蛋白质(Amyloid Precursor Protein,简称 APP)的形成,产生临床治疗效果,而且皆不需经由肝脏代谢,故不会造成肝毒性。另一類是 NMDA 受体(N-methyl-D-aspartate)拮抗剂 memantine(表一),memantine 可以防止 glutamate 的不正常传导,进而改善认知功能。 FDA核准用于中至重度阿兹海默症,是目前唯一治疗中度至中重度阿兹海默氏症的 NMDA 拮抗剂。
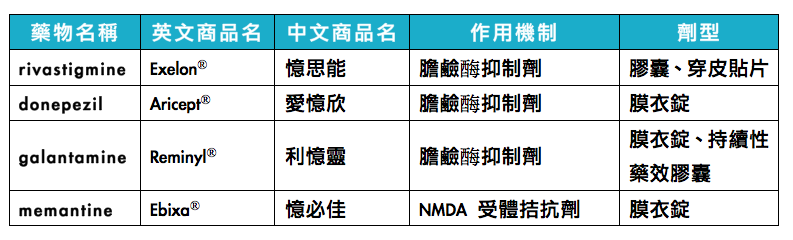
表一、台湾 FDA 核准治疗阿兹海默症的药物。(本表格由基因线上整理)
标靶类淀粉蛋白质的免疫疗法
免疫疗法主要是利用抗体来中和 β-类淀粉蛋白质(amyloid beta,简称 Aβ),治疗阿兹海默症,而依抗体产生的方式不同,可分成主动性免疫接种和被动性免疫接种二种。主动性免疫接种为借由疫苗刺激免疫系统而生成抗体。被动性免疫接种则是注射预制(pre-prepared)抗体。
主动性免疫接种参与细胞型和免疫体液型(humoral)免疫系统,具有成本效益和确保长期高抗体力价(antibody titers,代表抗体的含量)。最早主动免疫治疗阿兹海默症的疫苗为 AN-1792,利用全长的 Aβ 1-42 多肽作为免疫抗原直接进行免疫治疗,在小鼠实验中表现出了良好的治疗效果,但是在第二期临床试验中,引发严重的脑膜炎等副作用而被迫中止。目前许多第二代 Aβ 主动免疫疫苗正在进行第一期临床试验,包含诺华药厂(Novartis)研发 CAD106(Aβ1-6 多肽)、杨森药厂(Janssen)和辉瑞药厂(Pfizer)共同研发的 ACC001 (Aβ1-6 多肽)、AC 免疫研发的 ACI-24 (Aβ1-15 多肽)、默克药厂(Merck)研发的 V-950(Aβ1-15 多肽)、AFFiRiS 研发的 AD-02 (Aβ1-6 多肽)等。联脑科学 (United Neuroscience)所研发的 UB 311 (Aβ1–14多肽)已经进入第二期临床试验。
然而,主动性免疫接种会导致多株抗体反应,专一性较被动性免疫接种差,因此被动性免疫接种预防 Aβ 堆叠、清除 Aβ 的效果也较佳。目前进入第一期和第二期临床试验的抗体请见表二,而目前已经进行第三期临床试验的被动性免疫接种抗体,包含 Biogen 研发的 Aducanumab、AC 免疫研发的Crenezumab、罗氏(Roche)药厂研发的 Gantenerumab、礼来公司 (Eli Lilly)研发的 Solanezumab 等(表二)。
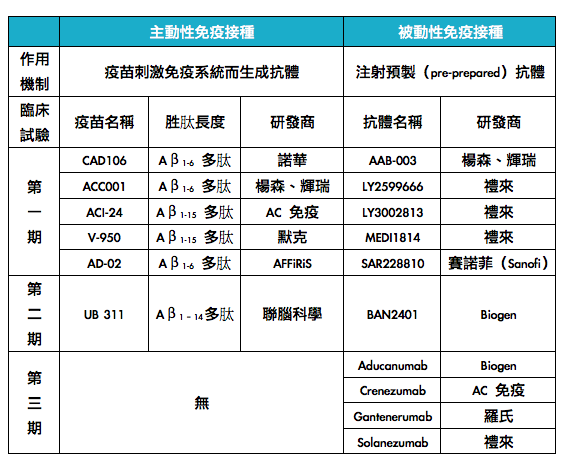
表二、主动性免疫接种和被动性免疫接种。(本表格由基因线上整理)
Tau 蛋白中心疗法
Tau 蛋白过度磷酸化促使阿兹海默症的发生及恶化,因此以 tau 蛋白为中心的疗法,包括 tau 蛋白激酶抑制剂、tau 蛋白堆叠抑制剂、微管稳定剂(microtubule stabilizers)和 tau 蛋白免疫疗法,都有可能治疗阿兹海默症(表三)。肝糖合成酶激酶-3(glycogen synthase kinase-3β,简称 GSK-3β)为 tau 蛋白磷酸化的最主要酵素,因此研究人员使用GSK-3β 抑制剂,如 tideglusib 和 AZD1080,进行临床试验,但结果显示,AZD1080 具有肾毒性(nephrotoxicity)会造成肾脏受损,而 tideglusib 于第二期临床试验结显示,没有安全性问题,但也无法证实有疗效。简言之,目前仍未有疗效佳且安全的 GSK-3β 抑制剂。
亚甲蓝(methylthioninium chloride)衍生物 LMTC 可抑制 tau 蛋白之间的交互作用,进而促使 tau 蛋白从脑部清除。微管稳定剂 BMS241027(epothilone-D)也可抑制 tau 蛋白堆积,虽然有进行第一期临床试验,但也已经终止。
目前 tau 蛋白免疫疗法,以预防神经纤维纠结(neurofibrillary tangles)形成为主要研究方向。Axon 神经科学公司所研发的 tau合成活性蛋白疫苗 AADvac1 和 AC 免疫与杨森共同研发的磷酸化 tau 蛋白特异性疫苗 ACI-35,皆能避免 tau 蛋白堆叠,目前分别进行入第二期和第一期临床试验。
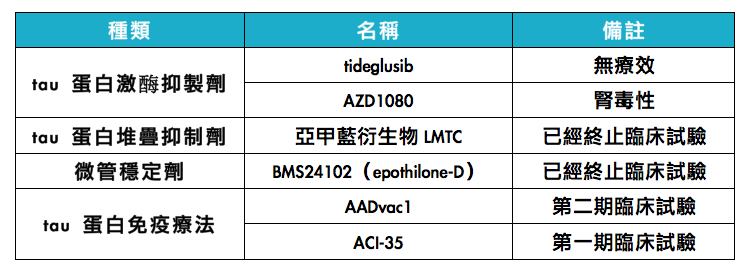
表三、Tau 蛋白中心疗法。( 本表格由基因线上整理)
参考资料:
1. Jan AT, et al. Front Aging Neurosci. 2017 Nov 1;9:356. doi: 10.3389.
2. http://dlweb01.tzuchi.com.tw/dl/med/joural/journal59.pdf
3. https://www.fda.gov.tw/mlms/hlist.aspx
4. https://wwwfs.vghks.gov.tw/001/VghksUploadFiles/288/ckfile/cf50b729-93c5-4dd4-9db9-97dd1ca68c07.pdf
5. https://www.alzforum.org/therapeutics
6. http://adisinsight.springer.com/drugs/800027767
7. https://www.sciencedirect.com/topics/medicine-and-dentistry/methylthioninium-chloride
8. Wang CY, et al. Alzheimers Dement (NY). 2017 Apr 14;3(2):262-272
9. Wischik CM J Alzheimers Dis. 2015;44(2):705-20.
©www.geneonline.news. All rights reserved. 基因线上版权所有 未经授权不得转载。合作请联系:service@geneonlineasia.com





