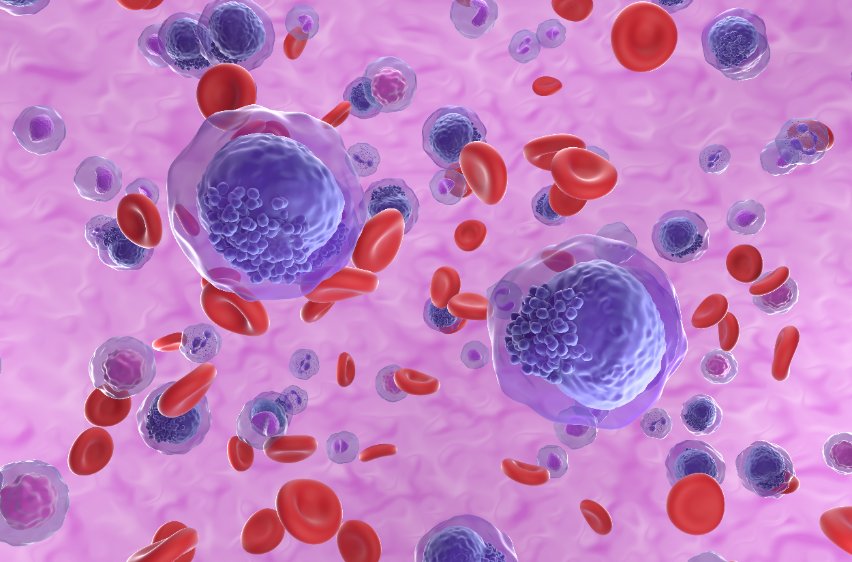
必治妥施貴寶(Bristol Myers Squibb, BMS)與 2seventy bio 共同研發的 Abecma(idecabtagene vicleucel)2021 年獲美國 FDA 核准,是第一個多發性骨髓瘤 CAR-T 療法,用於 4 線以上復發或難治型多發性骨髓瘤(multiple myeloma)成年患者。
近期兩公司以 Abecma 針對早期(2 線以後、4 線以前)多發性骨髓瘤患者試驗,初始試驗結果顯示,與標準治療方案相比 Abecma 顯著改善疾病無惡化存活期。儘管完整數據仍未公告,2seventy bio 表示這已有助於推動使 Abecma 用於患者的早期治療,也期待與監管單位遞交討論這些結果。
第一個 CAR-T 藥物 Abecma,目標拓展用藥族群
CAR-T 藥物 Abecma 透過結合多發性骨髓瘤 B 細胞高度表現的 BCMA 蛋白,以針對骨髓瘤細胞進行毒殺。自從 2021 年 3 月核准上市以來,2021 年約帶進 1.5 億美金銷售額,必治妥施貴寶、2seventy bio 預計今年全年銷售額更將攀升兩倍至 2.5-3 億間。
近期公告的 KarMMa-3 試驗數據,是一項評估 Abecma 的 3 期、全球、隨機多中心試驗,用於 2-4 線治療後復發和難治型早期多發性骨髓瘤成年患者,比較與 Darzalex, Pomalyst, Revlimid 等標準治療的治療效果。
初步結果達到主要療效指標,即疾病無惡化存活期(progression-free survival)顯著改善、完整數據仍未公開,次要療效指標的整體存活期(overall survival)表現仍在觀察進行中,預計今年下半年公告。安全性方面也與先前用於晚期患者的試驗結果一致,沒有出現新的安全疑慮。
血液性癌症 CAR-T 治療競爭激烈
今年 1 月,Abecma 剛在日本獲得厚生勞動省核准上市,必治妥施貴寶成為唯一在日本擁有兩項 CAR-T 細胞治療產品上市的生技藥廠,除 Abecma 外,另一細胞療法為標靶 CD-19 的 Breyanzi,主要治療二線以上多種類的大 B 細胞淋巴癌(LBCL),如瀰漫性大 B 細胞淋巴瘤(DLBCL)等。
今年 3 月,美國 FDA 批准第 2 項多發性骨髓瘤藥物 Carvykti,Carvykti 由 楊森(Janssen)藥廠與中國南京傳奇(Nanjing Legend Biotech)共同研發,也與 Abecma 核准條件一樣為 4 線以上復發或難治型多發性骨髓瘤。值得注意的是,楊森藥廠也正在進行 3 期試驗評估 Carvykti 用於早期患者療效。
延伸閱讀:緊追必治妥施貴寶!嬌生、南京傳奇聯手奪多發性骨髓瘤 CAR-T 藥證參考資料:
1. https://news.bms.com/news/corporate-financial/2022/Bristol-Myers-Squibb-and-2seventy-bio-Announce-Topline-Results-from-KarMMa-3-Trial-Showing-Abecma-idecabtagene-vicleucel-Significantly-Improves-Progression-Free-Survival-Versus-Standard-Regimens-in-Relapsed-and-Refractory-Multiple-Myeloma/default.aspx
2. https://clinicaltrials.gov/ct2/show/NCT04181827?term=ciltacabtagene+autoleucel&phase=2&draw=2&rank=3
©www.geneonline.news. All rights reserved. 基因線上版權所有 未經授權不得轉載。合作請聯繫:service@geneonlineasia.com