多重抗藥性(multidrug resistance, MDR)是造成抗生素效果逐漸降低主因,與藥物運輸排出的量增加、排入的量減少有關。美國麻省理工學院(MIT)化學研究團隊透過核磁共振(nuclear magnetic resonance, NMR)光譜,成功辨識出藥物運輸蛋白的結構是如何隨著藥物分子的移動而產生變化。未來將能藉抑制運輸蛋白結構的轉變以增加細菌的藥物敏感性。此研究於日前刊登於 Nature Communications。
抗藥性運輸蛋白 SMR 家族
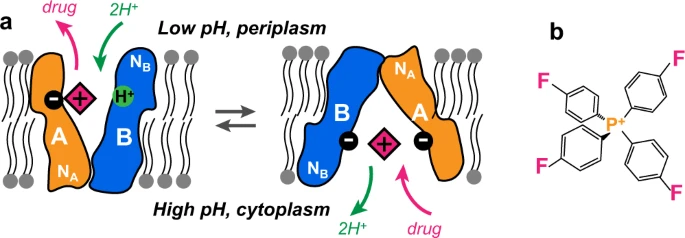
小分子多重抗藥性(small multidrug resistance, SMR)運輸蛋白家族透過在細菌細胞膜上高度表現,以增加藥物排出增加而導致抗藥性的產生。美國威斯康辛大學(University of Wisconsin)的 Henzler-Wildman 研究團隊多年來一直致力於 SMR 運輸蛋白家族中的 EmrE 的相關研究。EmrE 膜蛋白可以運輸多種有毒分子,包含除草劑和抗菌化合物等。據研究發現,EmrE 將有毒分子從細菌細胞內(酸鹼中性)運出細胞外(酸性),而 EmrE 的結構會根據酸鹼值的改變而產生變化,進而確保有毒分子皆排出於細胞外。
來自 MIT 化學研究團隊的 Mei Hong 教授的實驗室近期開發出全新技術,透過核磁共振技術以測量蛋白質中氟與氫原子的距離,進而辨識有含氟分子結合的蛋白質結構。Henzler-Wildman 進而提出利用 Mei Hong 團隊的核磁共振技術以探討 EmrE 如何跨磷脂質膜運輸藥物分子。
運輸蛋白隨酸鹼改變結構,增加藥物排出效率
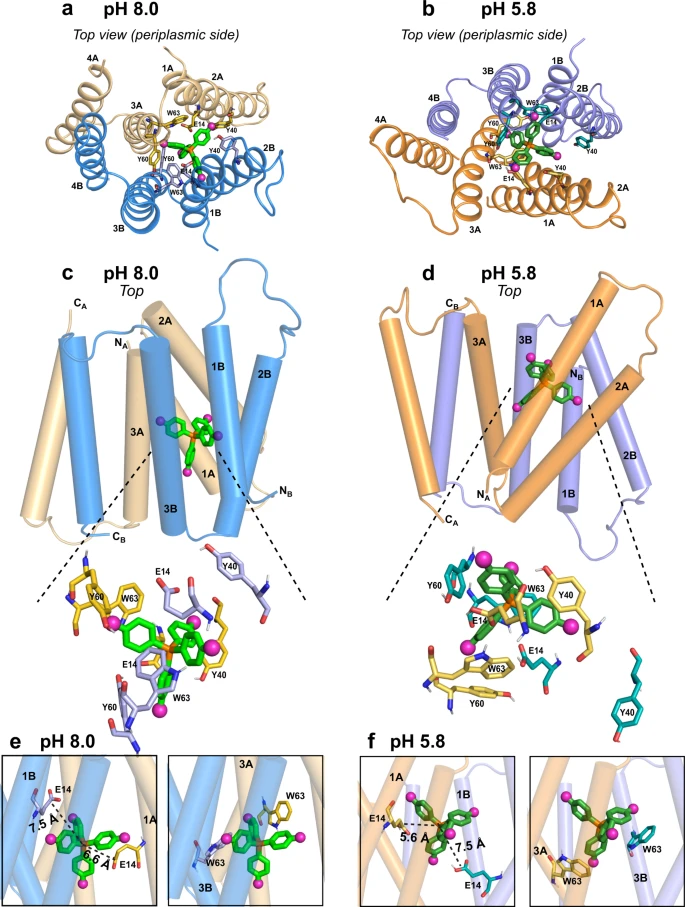
Hong 與 Henzler-Wildman的研究團隊 於 2021 年合作發表的文獻中指出,他們已成功透過核磁共振技術辨識出 EmrE 在酸性環境中的結構。而在本次發表的新研究中,成功分析出運輸蛋白在中性酸鹼值的結構,進而了解蛋白質的結構是如何在酸鹼值變化中改變以排出藥物分子。
在靠近細胞內、酸鹼呈中性時,組成運輸通道蛋白的四個螺旋體會排列成相對平行,進而形成一開口以方便藥物從細胞內進入通道。而隨著酸鹼值逐漸降低(變酸)時,螺旋體會排列呈傾斜狀,使通道向細胞外側更開放;與此同時,蛋白質側鏈的環狀結構也會隨著分子輸出細胞外而不斷改變,有利於藥物分子的輸出。
研究團隊指出,透過分析蛋白質運輸通道在酸性與中性的結構變化,可以更了解細菌是如何排除不利於自身的化學物質而產生抗藥性。未來也會持續針對運輸蛋白的結構變化做更多探討,以設計出抑制結構轉換的物質,進而改善抗藥性。
延伸閱讀:防堵細菌感染,用細菌載體攻破「生物膜」防護罩!參考資料:
1. https://www.nature.com/articles/s41467-022-28556-6
©www.geneonline.news. All rights reserved. 基因線上版權所有 未經授權不得轉載。合作請聯繫:service@geneonlineasia.com