癌症是許多基因突變造成細胞訊息傳遞路徑異常的結果,通常難以一次解決,而用藥時是否取得充足數據成為提升療效的關鍵。癌症治療需要診斷與療法的相互搭配,透過辨識癌細胞的分子特徵,來改變癌症藥物與診斷工具的開發過程。當今,已有不少能精準辨識癌症基因與分子的分析工具出現。
這些工具協助科學家辨識生物標記,找出癌症亞種分類,來正確選擇治療藥物,提升患者預後、找出受損路徑,也辨識促進疾病惡化的決定分子。
時下癌症精準醫療,包含診斷技術的進步:
- 從單位點檢測,變成多位點檢測
- 從低通量定序,提升至高通量定序
- 從多細胞檢測,演變至單細胞檢測
接下來將針對癌症精準醫療的檢測趨勢進行簡介,解密產業最熱門的工具與技術。
低通量到高通量、單位點到多位點
桑格定序法(Sanger sequencing)是最早用來辨識癌症突變的工具,但它相當耗時。次世代定序(NGS)的出現解決了應用痛點,整合聚合酶鏈反應(PCR)與螢光標記顯影(fluorescent labeling imaging),使科學家能掌握所有基因資訊,即時提供全面的腫瘤基因體樣貌。
目前已有多間企業投入腫瘤平台與伴隨式診斷工具的開發,透過 NGS 一次定序多種癌症突變。而這些 NGS 工具大約可分成 2 種類型:
- NGS 熱點檢測:辨識特定癌症患者體內的特定生物標記
- 全方位癌症基因檢測(CGP):全面檢測多種生物標記,取得相關研究數據
而近期出現的第 3 代單分子定序則無需經過 PCR 擴大流程,即可迅速定序目標的全基因體,取得基因與表觀遺傳學數據,可加速腫瘤分類與分析。
從多細胞到單細胞檢測
過去癌症檢測所使用的活體組織切片,常含有癌細胞與癌細胞附近的正常細胞,這會使小部分癌症的生物特徵難以被準確掌握。
不過,藉由高通量的定序單細胞基因、轉錄組(transcriptome)與表觀遺傳學,單細胞定序開始能分析具有異質性的腫瘤細胞。另外,這也推動了人類對腫瘤演進的理解,以及腫瘤產生化療抗藥性的背後機制。
除此之外,單細胞定序也擴大了腫瘤微環境的相關研究,進一步了解癌細胞成長的過程。而該常被用於研究腫瘤浸潤淋巴細胞(Tumor-infiltrating lymphocytes,TIL)的亞族群、譜系基準與功能狀態。
液態生物檢體登上檯面
目前,腫瘤的高異質性與演化速度大大阻礙了成功治癒機率的提升,而打破困境的要點之一就是取得廣泛的腫瘤樣本。然而,樣本得來不易,因為這往往需要透過侵入式手段取得,對患者來說非常不便。
近年來,液態生物檢體逐步證明了它能精準檢測腫瘤的能力。透過不侵入的取得血液樣本與後續分析,它可多次與動態的觀察腫瘤的演化,使其成為腫瘤內基因異質性(intratumor heterogeneity)的強大分析工具。
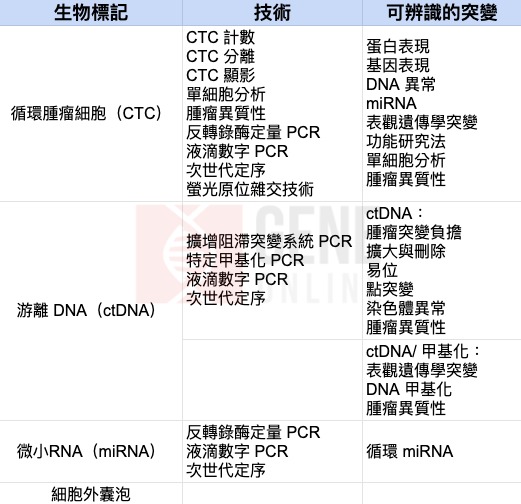
液態生物檢體會透過 PCR 或高通量定序,來檢測血液中腫瘤釋出的物質,譬如循環腫瘤 DNA(circulating tumor DNA, ctDNA)、循環腫瘤細胞(circulating tumor cells, CTCs)、胞外體(extracellular vesicles, EVs,又稱細胞外囊泡)與循環腫瘤 RNA(ctRNA)。
2020 年是癌症精準醫療的一大里程碑,因為當年 FDA 核准首 2 款液態生物檢體檢測工具,分別為 Guardant Health 的 Guardant360 CDx 和 Foundation Medicine 的 FoundationOne Liquid CDx。
該技術在腫瘤檢測、早期篩檢、即時腫瘤療法檢測、開發新療法、抗藥性機制研究與預測微量殘存疾病(MRD)風險等領域,皆具有臨床意義與應用。
然而,雖然該技術比傳統的組織切片更具技術優勢,但它仍需要更多研究來證實效力。且因部分研究指出,組織切片在一些癌症中能提供比液態切片更精準的結果,所以液態生物檢體還不能完全取代組織切片。
ctDNA
擴大、刪除與易位(translocations)ctDNA 對腫瘤早期篩檢、療法挑選、療法功效預測與預測腫瘤抗藥性與轉移有龐大的效益。
近年來,ctDNA 檢測工具一個一個出土,包含擴增阻礙突變系統(amplification refractory mutation system, ARMS)、微滴式數字聚合酶連鎖反應(Droplet digital polymerase chain reaction, DD PCR)與 NGS。
而 ctDNA 除了能用來辨識腫瘤突變,也可作為辨識腫瘤表觀遺傳改變的工具。ctDNA 的甲基化(methylation)可反應基因啟動子區域的過度甲基化特徵,也可利用腫瘤生物標記與特定組織的甲基化模式的訊號,來檢測與侷限(localize)腫瘤。另外,ctDNA 也可協助早期癌症檢測與患者預後評估,近期它也成為檢測微量殘存疾病,判斷癌症是否會復發的潛力工具。
CTCs
CTCs 是腫瘤在血液中剝落下來的細胞,是腫瘤轉移研究的基礎。且因為 CTCs 可被分離與擴大,所以 DNA 可用來分析腫瘤突變。
CTCs 可推動病原診斷、分子定序與疾病控管,同時也可用來改善治療策略選擇與預後判斷上。目前 FDA 僅核准 1 款 CTCs 檢測工具 CELLSEARCH® System,該工具能檢測 EpCAM、Cytokeratin、DAPI 和 CD45 等分子。
EVs
EVs 是可攜帶多種蛋白與核酸的脂質囊泡,它們能提供醫師患者腫瘤種類、腫瘤階段與轉移的資訊。
EVs 檢測能增加人類對腫瘤免疫逃脫反應(tumor immune escape)的了解,藉此加速可克服免疫抑制(immunosuppression)標靶療法的開發,胞外體液態切片工具比如 ExoDx Prostate IntelliScore,就已被 FDA 核准,能用於檢測前列腺癌與評估預後。
多體學思維
雖然用單體學取得的癌症數據不少,但它仍難以揭露分子特徵(molecular signatures)與癌症臨床特徵的關係。而透過整合基因、蛋白體學(proteomics)、表觀遺傳學的多體學數據,科學家則有機會理解疾病演化的因果和影響患者對療法反應的變數所在。而這也是癌症治療當今碰到的 2 大關卡。
近期,Greenleaf 與其同事整合 3 個單細胞定序技術 scRNA-seq、scATAC-seq 和 scCITE-seq 來讀取單血液細胞的總轉錄本(transcriptome)、表觀遺傳學與表面蛋白生物記號。研究團隊期望透過對比健康與白血病細胞的多體學數據,增進對辨別正常細胞與癌症細胞自我調節方式的了解。
此外,多體學數據能協助藥物開發、解釋療法反應與推動個人化醫療,使醫生順利找到標靶特定癌症的藥物。舉凡比利時 VIB-KU Leuven 癌症生物學中心的科學家早已在臨床上,將單細胞多體學技術應用在能阻礙癌細胞躲避免疫反應的檢查點抑制劑中,藉此了解為何患者會對療法產生不同反應。
癌症精準醫療挑戰
目前,許多癌症精準醫學工具已用於實驗室中,話雖如此,現實上該技術仍有不少臨床限制,使其難以進入市場。
第一,NGS 技術因樣本前處理的方式、平台、演算法不同,容易產生不穩定結果。
第二,單細胞定序的執行門檻高,需要新鮮的分離細胞外,實驗室設備的高要求,使研究人員無法進行廣泛的臨床研究。
第三,血液樣本雖可取代細胞切片來檢測腫瘤,但敏感度仍須改善,臨床上需要確認偽陽性,且最好使用液態生物檢體與活體組織切片 2 種檢測方式來檢測突變。
第四是 ctDNA 分析前樣本處理與純化缺乏標準指引,當今執行流程相當複雜,採取手段也容易降解該 DNA。
第五是 ctDNA 從血液中純化出來的技術挑戰。
第六是 CTCs 檢測相關的問題。
綜觀上述,儘管液態切片於一些研究被視為創新的癌症檢測,但實際上該技術仍需更多研究,才能奠定其在腫瘤診斷、控管與預後的產業與研究地位。
癌症精準醫療下一步
未來,表觀遺傳學、罕見基因檢測、個人化標靶療法與多基因標靶藥物領域中,精準檢測與整合檢測是研究趨勢之一。癌症精準醫學也將受益於雲端運算與 AI,這 2 項技術將用於分析多體學龐大的樣本與大數據。
而雖著數據量不斷增加,未來科學家也需思考標準化整合數據的方式。這除了技術進步要到位,也需要各領域的合作與連結,一起思考策略。
作者:Rajaneesh K. Gopinath
編譯:Tyler
參考資料:
1. https://geneonline.news/en/precision-oncology-overview-of-diagnostic-technologies/
©www.geneonline.news. All rights reserved. 基因線上版權所有 未經授權不得轉載。合作請聯繫:service@geneonlineasia.com






