十多年前,中國的專利保護仍是全球詬病之處。然而,近年來,中國在該領域進行大刀闊斧的改革,使得他們在 2019 年透過世界智慧財產權組織專利合作條約(Patent Cooperation Treaty, PCT)提交了5899 萬件專利申請,超越美國,成為提交全球專利申請量最多的國家,逐漸從專利權大國轉變為專利權強國。
截止 2019 年 8 月,全球醫藥專利約 960 多萬件,其中,化學藥占 28%,醫療器材佔 49%,其餘生物藥領域與中藥分別占 18% 與 5%。中國國內化學藥專利占 20%,中藥占 14%,生物藥占 11%。
中國醫藥市場概況
隨著專利權保護增加,也帶動了中國醫藥市場的成長,其 2019 年市場總值達到 16330 億人民幣(約 71626 億新台幣),年復合增長率為 7.5%,預計 2024 年達到 22288 億人民幣(約 96846 億新台幣)。該國目前已經成為全球第二大醫藥市場,僅次於美國。
臨床試驗和上市申請,化學藥占 8 成,生物藥占 14.6%
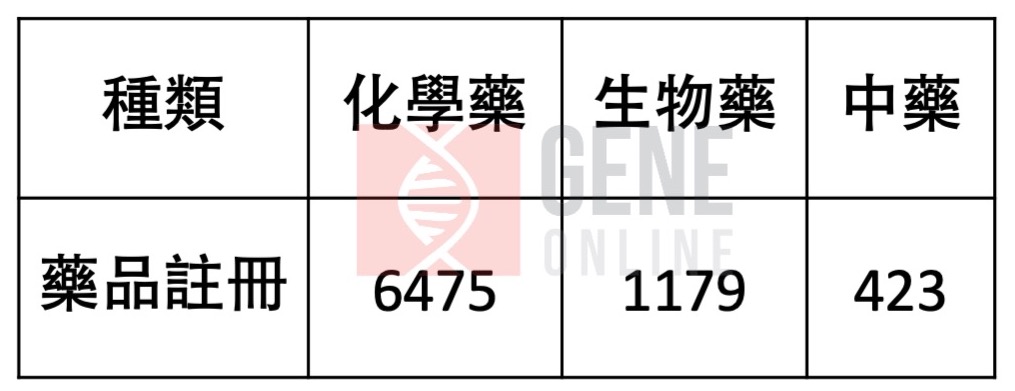
根據中國藥品監督管理局於 2020 年 7 月公布的「2019 年度藥品審查報告」,共有 8077 件藥品註冊申請,其中化學藥申請為 6475 件,佔該年度全部申請的 80.2%,生物藥申請為 1179 件,占 14.6%,中藥 423 件。
學名藥臨床試驗和上市申請仍佔多數,以抗腫瘤領域為主
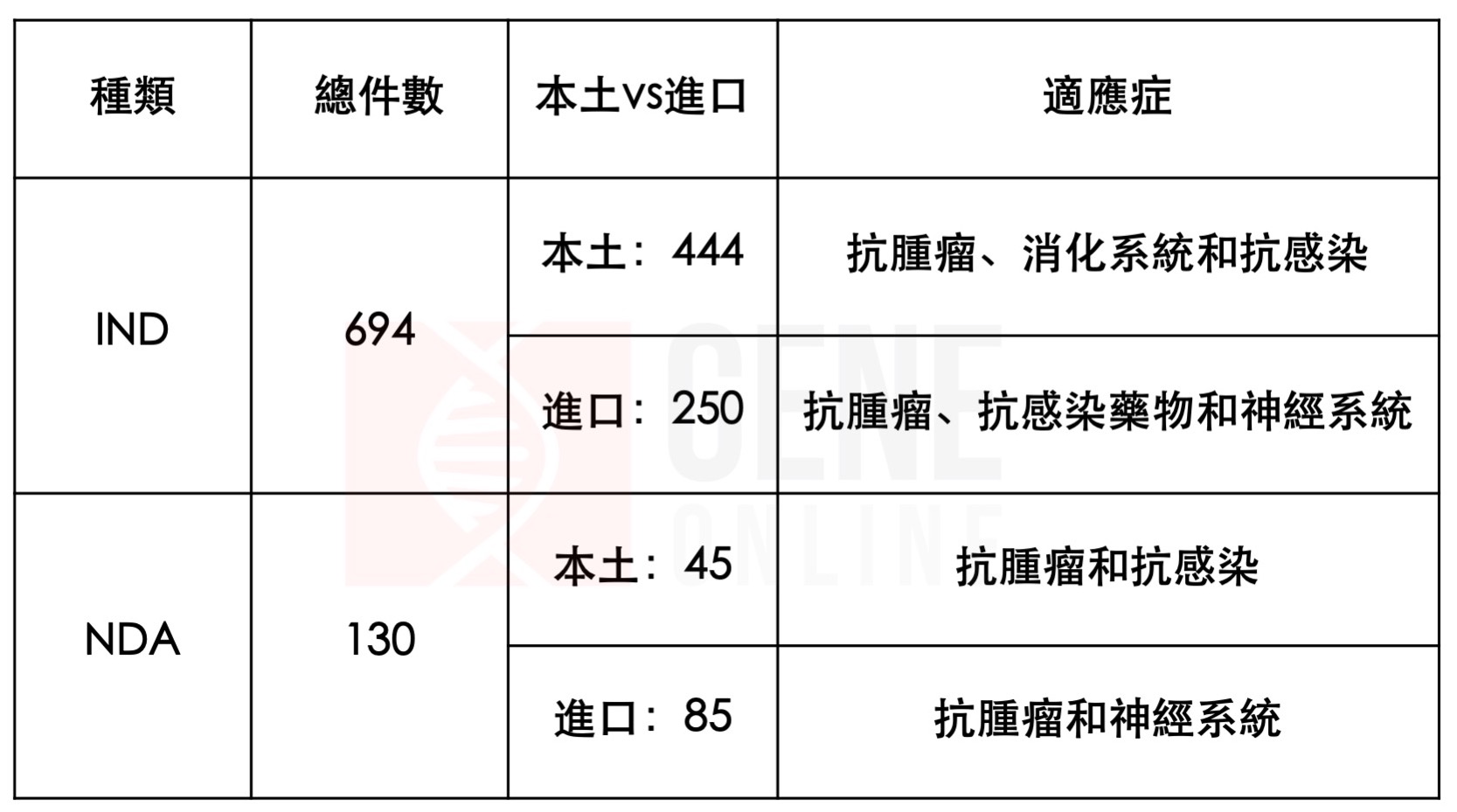
以化學藥申請為例,其中新藥臨床試驗(investigational new drug, IND)申請為 694 件,新藥查驗登記(new drug application, NDA)占 130 件,學名藥簡易新藥上市申請(abbreviated new drug application, ANDA)為 1047 件。
在化學藥 IND 申請中,中國本土 IND 為 444 件,進口 IND 申請為 250 件。中國 IND 本土適應症主要集中在抗腫瘤、消化系統和抗感染藥物領域,進口IND申請的適應症主要集中在抗腫瘤、抗感染藥物和神經系統領域。
在化學藥 NDA 中,中國本土 NDA 為 45 件,進口為 NDA 85 件。本土 NDA 的適應症主要集中在抗腫瘤和抗感染藥物領域,進口 NDA 的適應症主要集中在抗腫瘤和神經系統領域。
2019 年中國化學藥 IND 和 NDA 數量
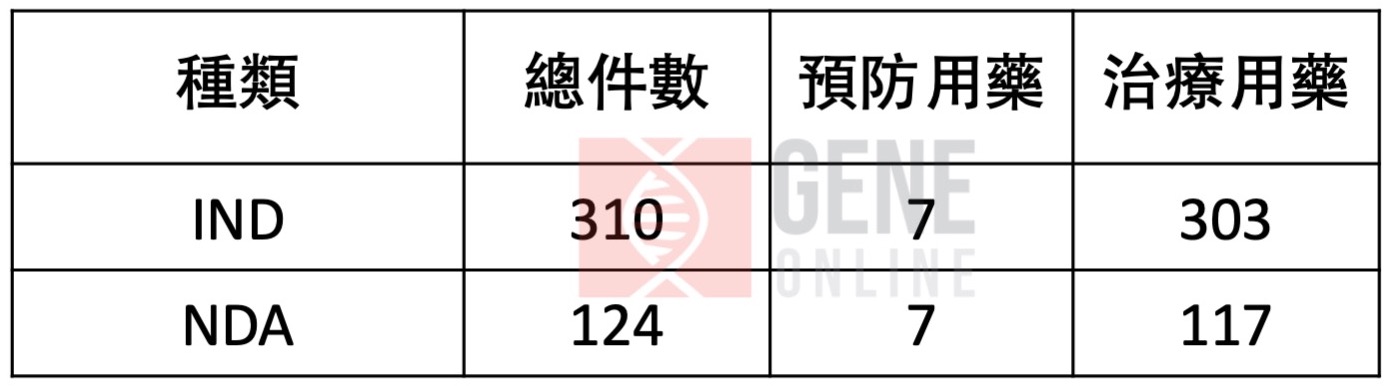
另外,生物藥申請共 1179 件,其中 IND 申請 310 件(預防用藥申請7件,治療用藥申請 303 件)。NDA 為 124 件(預防用藥申請 7件,治療用藥 117 件)。
2019 年中國生物藥 IND 和 NDA 數量
中國醫藥產業困境
由上述結果得知,中國醫藥企業仍以化學藥及學名藥為大宗,自主研發能力相對薄弱,低端產品比例大,缺乏具有專利權保護的特色新藥,且大多專注於本地市場,缺乏國外銷售管道,使得國際知名度低。
南京華訊知識產權顧問有限公司總經理侯慶辰博士對此表示:「想要推動中國醫藥產業從學名藥轉型為新藥開發,就必須克服研發資金大、週期長、失敗風險性高等問題,除了政府投資大量資金之外,最重要的是在專利法規上給予應用的專利權保障,否則在趨利避害的人性驅使下,必然很少有企業走向新藥開發的荊棘之路。」
延伸閱讀:2020 年中國新藥授權交易大爆發 延伸閱讀:中國專利法規改革帶動醫藥產業發展(下):專利連結制度、專利期限補償參考資料:
1. 中國衛生資源 2020, Vol. 23 Issue (3): 201-205, 216. DOI:10.13688/j.cnki.chr.2020.19371
2. https://www.nmpa.gov.cn/directory/web/nmpa/yaopin/ypjgdt/20200731114330106.html
3. 侯慶辰(2017)。論醫藥專利的產業化-中國專利法專題研究。翰蘆出版社。
©www.geneonline.news. All rights reserved. 基因線上版權所有 未經授權不得轉載。合作請聯繫:service@geneonlineasia.com





