急性骨髓性白血病(acute myeloid leukemia, AML)是由於血癌細胞抑制造血幹細胞分化,造成病患血球細胞數量不足與功能異常的疾病。台灣每年約增加 500 例新病例,是所有白血病中發生率最高的疾病類型,AML 的標準化療方式預後差,20 歲以上患者的五年存活率僅有 27%。
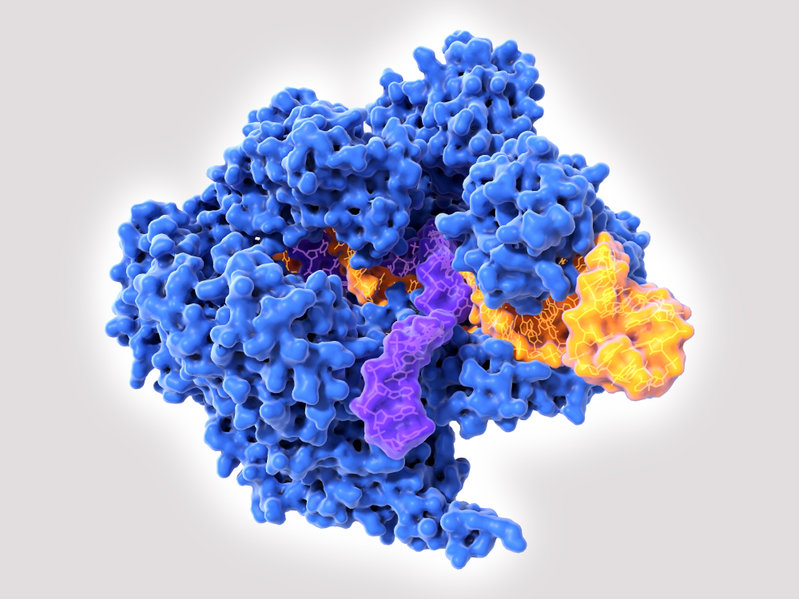
針對這項最難治療的白血病,賓州大學佩雷爾曼醫學院(Perelman School of Medicine at the University of Pennsylvania)團隊以 CRISPR 發現能抑制癌細胞增生的蛋白,並成功找出蛋白質上可與藥物分子結合的位點,研究團隊稱為「可成藥位點」(druggable pocket)的關鍵構造,相關結果刊登於《Molecular Cell》。
運用 CRISPR 標靶功能,找出抑制血癌細胞增生調節蛋白
CRISPR 最為人所知的功用是執行精準度高的 DNA 編輯,在這項研究中該團隊則應用 CRISPR 標靶基因的功能,大量篩檢導致 AML 的蛋白有執行功能的構造,以此作為開發藥物的標靶位點。
結果發現表觀遺傳調節蛋白 ZMYND8 會助長血癌細胞的增生。ZMYND8 透過一種纏繞在染色體上的組織蛋白(histone),它在不改變 DNA 序列的前提之下進行表觀遺傳修飾,進而促使癌細胞的基因表現與腫瘤轉移;相反的,如果在 AML 小鼠模型中抑制 ZMYND8 功能,則可提升小鼠存活率。
研究團隊也進一步指出 ZMYND8 蛋白調控的下游基因 IRF8,因此若要開發 ZMYND8 抑制劑的白癌藥物,可以從 IRF8 生物標記的表現量得知藥物成效。
標靶血癌致病蛋白的應用方向
此研究運用 CRISPR 的特性,找出助長血癌細胞增生的 ZMYND8 蛋白 ,因此透過抑制 ZMYND8 蛋白作用可以避免癌症擴散。
有別於目前許多癌症藥物都以突變基因為標靶對象,這項研究則標靶可抑制血癌細胞增生的蛋白,並且也指出受 ZMYND8 調控的下游生物標記基因,對於血癌藥物研發是一大突破。
延伸閱讀:兒童血癌治療新進展!Rylaze 獲 FDA 快速批准參考資料:
1. https://www.pennmedicine.org/news/news-releases/2021/august/crispr-screening-tool-identifies-new-drug-target-for-leukemia
2. Molecular Cell, 2021; https://www.cell.com/molecular-cell/fulltext/S1097-2765(21)00587-6
©www.geneonline.news. All rights reserved. 基因線上版權所有 未經授權不得轉載。合作請聯繫:service@geneonlineasia.com