近年来,基因疗法成为生物制药产业的热门产品,吸引不少企业家投资,也出现多起大型并购案,学术研究不断突破,临床试验结果更屡传捷报。据 Fortune Business Insights 统计,基因疗法市场规模在 2019 年约为 36.1 亿美元,预计将以 33.6% 的年复合成长率(CAGR)于 2027 年势如破竹达到 356.7 亿美元。
然而,这条路已从想像转为现实,并不总是那么乐观,仍有诸多技术与市场挑战。为了到达终点,基因疗法领域的研发人员必须忍受残酷的打击,需要重启站起,并持续创新摆脱危机。基因线上 GeneOnline 整理了基因疗法的开发历史、技术亮点以及应用挑战,带您迅速掌握来龙去脉。
基因疗法怎么传递到人体内?
基因疗法顾名思义就是引入健康基因或功能性基因到因缺陷基因引起的疾病患者中,达到治疗的效果。时下常提到的基因疗法,往往是细胞疗法与基因疗法的统称。这源自 2 种技术的领域有部分重叠,也因为多个著名的癌症免疫疗法譬如 CAR-T、TCR-T 皆会用到这 2 种技术制作,但这二者却截然不同。
据美国 FDA 定义,基因疗法是“所有透过转录或转译的遗传物质或整合到宿主基因体中来发挥功能的产品”,而执行方式大体可分 2 种类:活体外(Ex vivo)、活体内(In vivo)。
活体外基因疗法会把从患者体内取出的细胞,在实验室中重新编辑,最后再输回患者体内。而活体内基因疗法则是可直接将遗传物质送入活体内,或者透过病毒载体其他裸露 DNA、质体(plasmid)、奈米微脂体(lipid nanoparticle)等非病毒传递系统,将基因疗法进入体内增强或抑制缺陷基因,最著名的例子就是 CRISPR/Cas9。
其中,病毒载体是基因疗法常用的传递方式之一,举凡反转录病毒(retroviruses)、腺病毒(adenovirus)、单纯疱疹病毒(herpes simplex virus)、慢病毒(lentiviruses)、腺相关病毒(adeno-associated virus)等。
基因疗法的概念半世纪前就有了
基因疗法的概念发迹于 1960 年代,许多科学家正在假设其传递机制。1962 年,诺贝尔生理及医学奖得主 Joshua Lederberg 一封寄给美国医生 Stanfield Rogers 的信中写到,“相信不久之后,多核苷酸序列(polynucleotide sequences)将能透过科技接枝在病毒的 DNA 上”。
8 年后,Rogers 医生与 H. G. Terheggen 为了治疗精胺酸酶(arginase enzyme)缺乏的高精胺酸血症(hyperargininemia),将乳头状瘤病毒(Shope papillomavirus)传递至 2 位德国姐妹体内,使他们成为全世界第 1 个接受基因疗法的人类。
虽然从结果看来,这对姐妹对疗法并未产生反应,但 1972 年《Science》期刊上刊登的“Gene therapy for human genetic disease?”文章却成为基因疗法首个公认论文。
在众多支持者中,Theodore Friedmann 与 Richard Roblin 热烈支持基因疗法,并对当时的研究充满信心,但这没有蒙蔽他们的双眼,Theodore Friedmann 与 Richard Roblin 警告到基因疗法技术尚未成熟,在未全面理解基因调控、与疾病的关联前,尽量不要用在人类上,避免出现难以应付的副作用。
重组 DNA 技术出现
多年后,重组 DNA 技术(recombinant DNA technology)的出现推动了基因疗法的进程。1980 年,Martin J Cline 提出用重组 DNA 技术去治疗 2 位 β-地中海型贫血症(β-thalassemia)女性患者的计画,但因加利福尼亚大学洛杉矶分校(UCLA)的人类受试者保护委员会宣布禁止,所以该试验最后于美国外执行。之后,Cline 因违反联邦管制法规的人体试验规范被判刑。
第 1 个核准的基因疗法
时间走到 1990 年,基因疗法出现一大突破。美国国家癌症研究所(NCI)的 French Anderson、Michael Blaese 等研究员执行了世界第 1 个核准基因疗法。受试者是一位有着严重复合型免疫缺乏症(severe combined immunodeficiency, SCID),又称腺苷去胺酶(adenosine deaminase, ADA)缺乏的 4 岁孩童 Ashanti DeSilva。透过反转录病毒传递健康 ADA 基因,DeSilva 成为世上第 1 个成功被基因疗法治愈的人类。
因为他的成功,基因疗法的临床试验如雨后春笋冒出,也让 FDA 在 1993 年发布基因疗法相关规范。
声势浩大的基因疗法踢到铁板
基因疗法兴起研究热潮,许多人为了这神奇的医疗技术疯狂;然而,这些 90 年代的科学家接下来因临床试验困难、反转录病毒载体供给不足等挑战逐渐放弃,最后一击则是在 1999 年出现的第 1 个死亡事件。
Jesse Gelsinger 是一位 18 岁的美国患者,他自愿参加由宾州大学人类基因疗法中心创办人暨主任 James M Wilson 博士引导的临床试验。该试验主要以腺病毒相关基因疗法来治疗罕见基因疾病——鸟胺酸氨甲酰基转移酶缺失(Ornithine Transcarbamylase Deficiency)婴儿患者的效益。这种罕见疾病会使人无法代谢血液中的氮,并在出生时迅速致死,不过 Gelsinger 拥有症状较轻的鸟胺酸氨甲酰基转移酶缺失且活至成年,所以被判定为十分合适的受试者。
试验开始后马上急转直下,Gelsinger 注射最高剂量后即刻发高烧,接下来数日出现黄疸症状,暗示著肝脏毒性过高。4 日后,Gelsinger 死于严重的免疫反应,包含多重器官衰竭与脑死。
这一个死亡事件促使 FDA 等多个单位对 Wilson 博士提出控诉,违反临床试验相关规范,不仅让他的基因疗法职涯走向终点,也重重打击了基因疗法界,随后几个月内,基因疗法临床试验的数量骤降。
记取教训,基因疗法死灰复燃
诉讼同时,Wilson 与其团队针对 Gelsinger 致死的原因进行研究,他们发现 Gelsinger 早已接触过腺病毒,所以在基因疗法进入体内时,Gelsinger 的免疫系统产生了严重的发炎反应。
另外,Wilson 也向密西根大学医学院教授 Tachi Yamada 寻求意见。Yamada 建议他应继续研究基因疗法,并解决问题来源;这一个会面间接成为了基因疗法研究的转捩点,因为 Wilson 后来研发出不会引发致命免疫反应的腺相关病毒载体(AAVs),也就是时下基因疗法最常使用的病毒载体之一。
AAVs 载体的活跃
AAVs 最早于 1965 年被鉴定为腺病毒制剂中的污染物。虽然 AAVs 在转导效益上比腺病毒来的低,但却表现出低致病性、能长时间维持基因表现的特性,且 AAVs 的免疫原性也相对较低。
Wilson 随即将次世代 AAVs 的开发任务交予当年的博士后研究员 Guangping Gao。Gao 博士当时正在研读 AAV 原型,譬如 AAV2,但在 Gelsinger 死亡事件后将研究焦点转往病毒载体的安全性。Gao 后来研究出一个能从非人类灵长类中取得多样 AAVs 的技术,且这些病毒载体都未表现出严重的免疫反应。而 Gao 现在已成为宾州大学人类基因疗法中心的副主任。
时至今日,AAVs 被视为基因疗法的黄金标准,高度用于临床试验中。该技术不仅安全性高、组织向性广泛、致病性低,且能有效的做到基因传递。
2012 年,欧洲药品管理局(EMA)核准了全球第 1 个 AAV 基因疗法 Glybera 用于治疗脂蛋白脂肪酶缺乏(lipoprotein lipase deficiency)患者。直到今日(2021/03/06),FDA 则核准 2 个 AAV 基因疗法,分别是 Novartis 治疗脊髓性肌肉萎缩症的 Zolgensma 和 Spark Therapeutics 治疗莱伯氏先天性黑蒙症的 Luxturna。
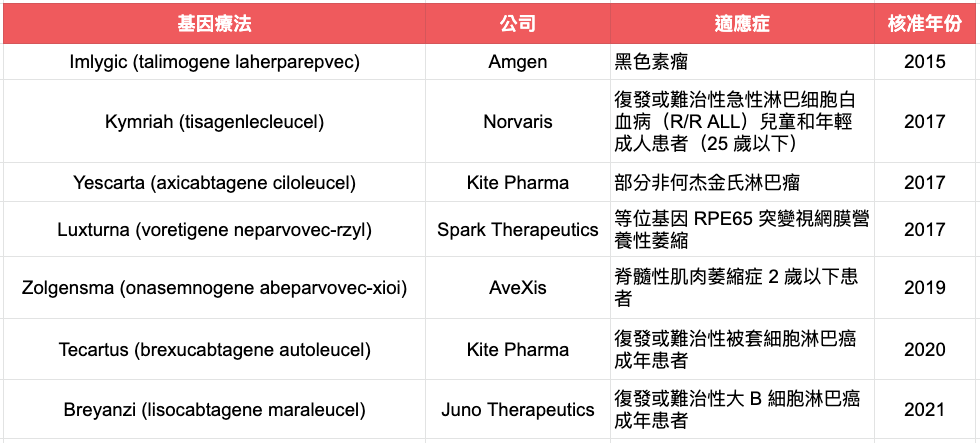
基因疗法潜力无穷,但距离普及还有一大段路
除了上述已核准上市的 AAV 基因疗法之外,它治疗遗传性疾病、罕见单基因疾病、癌症、帕金森氏症、亨丁顿氏舞蹈症等研究和临床试验也在进行中;其中,大多是肿瘤癌症领域。因应此热潮,FDA 估计会在 2025 年前通过 10 至 20 个细胞、基因疗法。
另外,CRISPR/Cas9 的出现扩大了基因疗法领域的应用层面,这把“基因剪刀”可望让临床研究人员能更精准、更简单的编辑基因。近期在 CRISPR Therapeutics 与 Vertex Pharmaceuticals 合作中的临床试验中,他们使用 CRISPR/Cas9 基因编辑后的造血干细胞 CTX001 来治疗 β-地中海型贫血症与镰刀型红血球疾病(sickle cell disease),结果表现正面。
然而,安全性与制造成本仍有许多障碍要排除。首先,目前仍有研究指出 AAVs 多少还是会引发免疫反应,并在部分患者中产生免疫介导毒性。为此,许多研究团队正在进一步改造 AAVs 来帮助它躲过宿主的免疫系统。另外,基因疗法的制作成本高昂,难以用亲民的价格普及于大众市场,而这可能让患者无法取得治疗,更会使开发公司无法获得足够经费,支持技术创新。例如,Glybera 费用是 100 万美元,全世界最贵药物,患者不买单,最后失败退出市场。
然而,基因疗法仍是时下最具潜力的疗法之一,只要整合好药物开发、产品线与商业化技术,未来潜能可期。
掌握基因疗法基础后,接下来 GeneOnline 三月专题将带您了解 2021 年 10 大基因疗法公司,掌握最新产业动态。
作者:Rajaneesh K. Gopinath
编译:Tyler

©www.geneonline.news. All rights reserved. 基因线上版权所有 未经授权不得转载。合作请联系:service@geneonlineasia.com